¶ Fármacos Antagonistas Alfa–Adrenérgicos
Carrera de Medicina – Facultad de Ciencias Químicas y de la Salud (UTMACH)
Autores: Viviam M. Ibañez C.; Jefferson F. Quezada F.; Paula C. Peláez C.
Docente: Dr. Roberto Eduardo Aguirre Fernandez PhD.
¶ 📄 Introducción
Los bloqueadores α-adrenérgicos representan una clase de fármacos cuyo mecanismo de acción se basa en la inhibición competitiva de los receptores α₁ o α₂ adrenérgicos, limitando la respuesta vasoconstrictora mediada por catecolaminas. [1] Esta acción se traduce en una reducción de la resistencia vascular periférica y en la consecuente disminución de la presión arterial, además de efectos directos sobre el músculo liso prostático y la uretra, lo que explica su utilidad en trastornos urinarios obstructivos. [2]
Durante la última década, diversas guías y revisiones sistemáticas han evaluado de manera rigurosa el papel clínico de los antagonistas α₁, especialmente en el tratamiento de la hiperplasia prostática benigna (HPB) y de los síntomas del tracto urinario inferior (STUI). [3] La evidencia reciente ha confirmado su eficacia para mejorar el flujo urinario, reducir la puntuación IPSS y mejorar la calidad de vida, con un perfil de seguridad aceptable en población adulta. [4] Sin embargo, el uso de estos fármacos como agentes antihipertensivos ha sido reevaluado, ya que su empleo como tratamiento de primera línea no se recomienda debido al mayor riesgo de hipotensión ortostática, síncope y eventos cardiovasculares comparado con otras clases terapéuticas. [5]
La seguridad de los bloqueadores α-adrenérgicos en poblaciones vulnerables, como adultos mayores, ha recibido especial atención. Metaanálisis recientes han evidenciado un aumento significativo del riesgo de caídas, mareos y efectos adversos relacionados con la vasodilatación en pacientes mayores de 65 años, lo que obliga a una selección más estricta y a un monitorio clínico cuidadoso en este grupo etario. [6] Asimismo, estudios observacionales de gran escala han identificado asociaciones entre la administración de antagonistas α₁ y potenciales beneficios en contextos no tradicionales, incluyendo una menor mortalidad intrahospitalaria en hombres hospitalizados por COVID-19, posiblemente mediada por efectos inmunomoduladores y antiinflamatorios. [7]
Por otra parte, investigaciones farmacodinámicas recientes han mostrado diferencias sustanciales entre los distintos agonistas α₁ en cuanto a selectividad (α₁A/α₁B/α₁D), semivida, efectos metabólicos y perfil hemodinámico, lo cual es determinante para su aplicación terapéutica. [8] Agentes altamente selectivos como tamsulosina y silodosina han demostrado menor riesgo de hipotensión ortostática al compararse con antagonistas no selectivos como doxazosina o terazosina, lo que ha orientado las recomendaciones clínicas actuales en urología. [9]
En conjunto, la literatura contemporánea subraya la relevancia clínica de los bloqueadores α-adrenérgicos, tanto por su eficacia en los STUI asociados a HPB como por los retos que plantea su seguridad cardiovascular y neurológica en poblaciones específicas. [10]
¶ 🧬 Desarrollo
¶ Clasificación de los bloqueadores adrenérgicos
Los receptores adrenérgicos α se dividen en α₁ (α₁A, α₁B, α₁D) y α₂ (α₂A, α₂B, α₂C), cada subtipo se acopla a un tipo específico de proteína G, lo que determina el tipo de respuesta fisiológica que generan. [11] En términos generales:
- Los receptores α₁ (acoplados a Gq) → generan vasoconstricción.
- Los receptores α₂ (acoplados a Gi/o) → regulan la liberación de noradrenalina y también pueden generar vasoconstricción en su subtipo α₂B, pero su función central es inhibitoria presináptica. [12]
El bloqueo farmacológico de estos receptores produce efectos opuestos:
- Bloqueo α₁ → vasodilatación.
- Bloqueo α₂ → aumento del tono simpático y, por tanto, taquicardia y en ocasiones vasoconstricción refleja. [13]
¶ Bloqueadores selectivos α₁-adrenérgicos
Los receptores α₁ adrenérgicos se acoplan a la proteína Gq/11, cuya activación estimula la fosfolipasa C (PLC). Esto genera un aumento de IP₃ y DAG, elevando el calcio intracelular. [14] El incremento de Ca²⁺ activa la calmodulina y la MLCK, produciendo contracción del músculo liso, especialmente en vasos sanguíneos, lo que contribuye a la vasoconstricción y al aumento de la resistencia vascular periférica. [15]
Efecto fisiológico del receptor α₁:
- Vasoconstricción
- Aumento de la resistencia vascular
- Incremento de la presión arterial
- Contracción de músculo liso uretral y prostático
Efecto del bloqueo farmacológico de α₁:
- Vasodilatación arterial y venosa
- Disminución de la resistencia vascular sistémica
- Relajación del tracto urinario inferior
¶ Antagonistas selectivos α₁A
El subtipo α₁A se expresa principalmente en la próstata, la uretra y el cuello vesical, su activación incrementa el tono del músculo liso en estas estructuras, favoreciendo la contracción y contribuyendo a fenómenos como la obstrucción del tracto urinario inferior, especialmente en la hiperplasia prostática benigna. [16]
Características principales:
- Relajan selectivamente el músculo liso prostático.
- Mucho menor impacto hemodinámico.
- Rara vez producen hipotensión, muy útiles en pacientes ancianos.
¶ Bloqueadores selectivos α₂-adrenérgicos
Los receptores α₂ adrenérgicos se acoplan a proteínas Gi/o, cuya activación inhibe el adenilato ciclasa, provocando una disminución del cAMP. [17] Esto reduce la actividad de la PKA, disminuye la entrada de Ca²⁺ a través de canales voltaje-dependientes y, como consecuencia, reduce la liberación de noradrenalina desde las terminales nerviosas presinápticas. [18] Este mecanismo ejerce un importante efecto inhibidor modulador dentro del sistema nervioso simpático como veremos a continuación. [19]
Efecto fisiológico de los receptores α₂:
- Autoinhibición simpática presináptica
- Disminución de la liberación de noradrenalina
- Reducción de la frecuencia cardíaca
- Vasoconstricción
Efecto del bloqueo farmacológico de α₂:
- Aumento de la liberación de noradrenalina
- Mayor tono simpático
- Taquicardia y aumento del gasto cardíaco
- Elevación de la presión arterial
¶ Bloqueadores no selectivos
Antagonizan simultáneamente los receptores α₁ y α₂ adrenérgicos, bloqueando tanto los efectos postsinápticos mediados por α₁ como los efectos presinápticos mediados por α₂. [20]
- Bloqueo α₁ → vasodilatación marcada (Disminución de la resistencia vascular, Descenso de la presión arterial).
- Bloqueo α₂ → liberación masiva de noradrenalina (Taquicardia intensa, Hipertensión refleja, Aumento del gasto cardiaco).
Por ello, pese a causar vasodilatación, estos fármacos pueden producir un aumento marcado del tono simpático. [21]
Los antagonistas α-adrenérgicos se dividen en reversibles e irreversibles, según el tipo de unión que establecen con el receptor.
- Los antagonistas reversibles: como la fentolamina y la tolazolina, se unen de manera no covalente, por lo que su efecto puede ser desplazado por concentraciones elevadas de catecolaminas. [22] Se caracterizan por un inicio de acción rápido y una duración corta, lo cual los hace útiles en situaciones agudas como las crisis hipertensivas inducidas por liberación excesiva de catecolaminas. [23] Sin embargo, su uso puede acompañarse de efectos adversos importantes, especialmente taquicardia marcada y arritmias debido al aumento del tono simpático reflejo. [24]
- Los antagonistas irreversibles: representados principalmente por la fenoxibenzamina, se unen de forma covalente al receptor α y generan un bloqueo prolongado que solo se revierte cuando se sintetizan nuevos receptores. [25] Este perfil farmacológico los convierte en fármacos clave para el manejo preoperatorio del feocromocitoma, ya que evitan las oscilaciones hipertensivas causadas por descargas de catecolaminas. [26] No obstante, su acción sostenida incrementa el riesgo de hipotensión prolongada, especialmente en pacientes con volumen intravascular reducido. [27]
¶ Tabla 1: Clasificación de Antagonistas Alfa-Adrenérgicos
| Receptor | Proteína G | Efecto fisiológico | Tipo de acción vascular | Efecto del bloqueo |
|---|---|---|---|---|
| α₁A / α₁B / α₁D | Gq/11 | Aumenta Ca²⁺, contrae músculo liso | Vasoconstricción | Vasodilatación |
| α₂A / α₂C | Gi/o | Disminuye liberación de NA (inhibitorio) | Indirecto (reducción simpática) | Aumento del tono simpático |
| α₂B | Gi/o | Vasoconstricción directa en vasos | Vasoconstricción | Vasodilatación leve + aumento de NA |
| No selectivos (α₁ + α₂) | Gq y Gi | Efecto mixto | Vasodilatación + Hipersimpaticotonía | Vasodilatación + Taquicardia |
¶ Mecanismo de acción de los bloqueadores α-adrenérgicos (α₁ y α₂)
Los antagonistas adrenérgicos α constituyen un grupo farmacológico cuya acción principal consiste en inhibir la señalización mediada por los receptores α₁ y α₂, modulando así múltiples funciones cardiovasculares, autonómicas y metabólicas. [28] Dado que los receptores adrenérgicos α participan tanto en mecanismos postsinápticos como presinápticos, su bloqueo genera efectos fisiológicos distintos y, en algunas situaciones, complementarios. [29]
1. Bloqueadores α₁-adrenérgicos
Los receptores α₁ se acoplan a proteínas Gq/11, activando la fosfolipasa C y promoviendo la formación de IP₃ y DAG, lo que estimula un aumento de Ca²⁺ intracelular y la contracción del músculo liso vascular. [30] Su bloqueo inhibe esta cascada, disminuyendo la disponibilidad de Ca²⁺ y generando relajación del músculo liso. [31]
Este proceso explica la acción antihipertensiva de los antagonistas α₁, que producen vasodilatación arterial y venosa, reducen la resistencia vascular sistémica y la presión arterial. [32] A nivel urológico, el bloqueo del subtipo α₁A, predominante en la próstata y cuello vesical, disminuye el tono del músculo liso y mejora el flujo urinario en la hiperplasia prostática benigna. [33]
Estudios estructurales recientes han descrito con detalle las conformaciones del receptor α₁A y la forma en que los antagonistas estabilizan la forma inactiva del receptor e impiden el acoplamiento interno a la proteína Gq. [34] Este hallazgo ha permitido desarrollar fármacos con mayor selectividad, destinados a minimizar la hipotensión ortostática y otros efectos hemodinámicos adversos. [35]
Asimismo, se ha demostrado que los receptores α₁ participan en rutas de señalización no clásicas independientes de Gq, incluyendo vías reguladas por PKC, Src y canales de Ca²⁺ tipo Cav1.2. [36] Esto sugiere que el antagonismo podría modular funciones más amplias que la simple contracción del músculo liso, como la modulación neuronal y cardiomiocitaria. [37]
2. Bloqueadores α₂-adrenérgicos
Los receptores α₂ están acoplados a proteínas Gi/o y desempeñan un papel regulador inhibitorio sobre la neurotransmisión adrenérgica. [38] Su activación presináptica inhibe el adenilato ciclasa, disminuye el cAMP, reduce la entrada de Ca²⁺ y suprime la liberación de noradrenalina como mecanismo de retroalimentación negativa. [39]
Cuando estos receptores son bloqueados, se elimina este control inhibitorio, lo que provoca:
- Aumento de la liberación de noradrenalina, al liberarse la inhibición presináptica. [40]
- Incremento del tono simpático, manifestado clínicamente con taquicardia, elevación del gasto cardiaco y aumento moderado de la presión arterial. [41]
- Hiperestimulación postsináptica de receptores β y α₁, dado el exceso de noradrenalina disponible. [42]
Además del control autonómico, los receptores α₂A desempeñan un papel metabólico importante inhibiendo la secreción de insulina en células β pancreáticas. Por ello, el bloqueo α₂ puede potenciar la liberación de insulina, un efecto demostrado en estudios recientes sobre regulación metabólica simpatoadrenérgica. [43]
En el sistema nervioso central, el bloqueo de α₂ puede aumentar la excitabilidad neuronal y modular funciones relacionadas con el dolor, la cognición y la respuesta al estrés. [44] Este mecanismo explica el uso limitado de antagonistas α₂ a fármacos específicos, empleada como herramienta experimental para estudiar la función simpática y en ciertos trastornos vasculares. [45]
3. Bloqueo combinado de α₁ y α₂
Los antagonistas no selectivos actúan tanto sobre α₁ como α₂, al bloquear α₁ producen vasodilatación, pero la inhibición simultánea de α₂ presinápticos induce una liberación exagerada de noradrenalina, lo que causa: [46]
- Taquicardia intensa
- Aumento del gasto cardíaco
- Actividad simpática exacerbada
Estos efectos justifican su uso casi exclusivo en situaciones particulares como el manejo preoperatorio y las crisis hipertensivas del feocromocitoma, donde se requiere antagonizar la acción catecolaminérgica masiva. [47]
Consideraciones fisiológicas y farmacológicas relevantes
El entendimiento actual reconoce que los efectos de los bloqueadores α no solo dependen del receptor objetivo, sino también de:
- Distribución tisular diferencial de los subtipos
- Selectividad del fármaco
- Afinidad por el receptor
- Capacidad de producir antagonismo competitivo o irreversible
Los antagonistas irreversibles como la fenoxibenzamina bloquean de manera prolongada la respuesta al tono simpático, lo que confiere ventaja en feocromocitoma, pero aumenta el riesgo de hipotensión prolongada. [48] Por el contrario, los antagonistas competitivos selectivos de α₁ permiten una modulación más controlada del tono vascular con menor repercusión autonómica. [49]
¶ 🏥 Aplicaciones clínicas de los bloqueadores α-adrenérgicos
¶ 1. Bloqueadores α₁
Los antagonistas α₁ son los más utilizados clínicamente, por sus efectos sobre la vasodilatación y la relajación del músculo liso prostático:
- Hipertensión arterial: Los α₁-bloqueadores pueden utilizarse como terapia complementaria en el tratamiento de la hipertensión, y en la práctica clínica se emplean con mayor frecuencia en pacientes con hipertensión resistente o cuando se busca un beneficio adicional en pacientes que además tienen síntomas urinarios por HPB. [50] Estudios y revisiones recientes reconocen que, si se combinan de forma adecuada con otros fármacos antihipertensivos, los α₁-bloqueadores pueden controlar la tensión arterial de forma segura, aunque no suelen ser fármacos de primera línea para la mayoría de los pacientes. [51] Sin embargo, hay evidencia histórica que advertía de un aumento en la incidencia de insuficiencia cardíaca en el brazo con doxazosina, motivo por el cual ese brazo se suspendió prematuramente; por tanto, su uso exige consideración cuidadosa en pacientes con alto riesgo cardiovascular y seguimiento. [52]
- Hiperplasia prostática benigna (HPB) / LUTS: Los α₁-bloqueadores son tratamiento de primera línea para los síntomas del tracto urinario inferior secundarios a HPB: reducen el tono del músculo liso prostático y del cuello vesical, mejoran el flujo urinario y disminuyen la puntuación del IPSS. [53] Existen fármacos más uroselectivos como tamsulosina, silodosina, alfuzosina, que tienden a tener menor efecto hipotensor sistémico en comparación con agentes no selectivos, la elección se individualiza según comorbilidades, tolerancia y preferencia del paciente. [54]
- Utilización en oncología: Hay evidencia preclínica y observacional que sugiere efectos antitumorales de ciertos α₁-bloqueadores sobre líneas celulares prostáticas y modelos animales: se han descrito inducción de apoptosis, inhibición de proliferación y efectos sobre la migración/invasión tumoral. [55] Estos hallazgos han motivado interés por su potencial uso como terapia complementaria o de repurposing en tumores como el de próstata o riñón, pero la evidencia clínica robusta y los ensayos controlados en humanos son todavía limitados, por lo que por ahora su aplicación en oncología sigue siendo experimental. [56]
- Pantalla / preparación preoperatoria de feocromocitoma: En la preparación para resección de feocromocitoma, el bloqueo α es un pilar del manejo hemodinámico. [57] Aunque el fenoxibenzamina es clásico, los α₁ selectivos orales se utilizan con frecuencia en la práctica clínica para estabilizar la presión arterial antes de la cirugía en muchos centros, especialmente cuando se busca una alternativa con menos efectos adversos a largo plazo. [58]
- Efectos sobre la función sexual: Los α-bloqueadores pueden afectar la función sexual, sobre todo la eyaculación. Algunos se han asociado con mayores tasas de trastornos eyaculatorios, debido a la relajación del cuello vesical y de la musculatura prostática. [59] También se han descrito cambios en libido y, raramente, priapismo, las diferencias entre agentes uroselectivos vs no selectivos influyen en el perfil de riesgo. Es recomendable discutir estos efectos con el paciente antes del inicio del tratamiento. [60]
¶ 2. Bloqueadores α₂
Los antagonistas de los receptores α₂ tienen aplicaciones más limitadas en la práctica clínica actual, pero son relevantes en ciertos contextos:
- Investigación del tono simpático: Los antagonistas adrenérgicos, especialmente los bloqueadores α₂, se emplean en estudios fisiológicos y experimentales para investigar la regulación presináptica de la liberación de noradrenalina. [61] Al bloquear los receptores α₂ presinápticos, se elimina el mecanismo de retroalimentación negativa normalmente responsable de limitar la exocitosis de neurotransmisores. [62] Esto permite observar cambios en el tono simpático basal, la dinámica de liberación de noradrenalina y las respuestas cardiovasculares y autonómicas derivadas, siendo herramientas útiles en investigación neurofarmacológica y en modelos animales. [63]
- Disfunción eréctil de origen vascular: En algunos casos seleccionados, la yohimbina, un antagonista selectivo de los receptores α₂, se utiliza como coadyuvante para tratar la disfunción eréctil de probable origen vascular o neurogénico. [64] Su mecanismo se basa en el aumento de la liberación de noradrenalina y en la reducción del tono simpático periférico, lo que puede favorecer el flujo sanguíneo peneano. [65] No obstante, su eficacia es modesta, su ventana terapéutica es estrecha y puede generar efectos adversos relevantes, por lo que no constituye un tratamiento de primera línea frente a los inhibidores de la fosfodiesterasa tipo 5. [66]
- Reversión de efectos de sedantes α₂: En medicina veterinaria, antagonistas específicos de los receptores α₂ se emplean para revertir la sedación, analgesia y bradicardia inducidas por agonistas α₂. [67] Estos antagonistas desplazan al agonista del receptor, restaurando el tono simpático normal y acelerando la recuperación del animal, su uso es fundamental para controlar la duración de la sedación y mejorar la seguridad perioperatoria en procedimientos diagnósticos o quirúrgicos. [68]
¶ 3. Bloqueadores no selectivos (α₁ + α₂)
Estos fármacos antagonizan ambos subtipos α y tienen aplicaciones específicas por su perfil de acción combinado:
- Feocromocitoma: En la preparación para la cirugía del feocromocitoma se emplean bloqueadores α no selectivos para controlar la hipertensión inducida por catecolaminas. [69]
- Fenoxibenzamina: antagonista irreversible, útil para un bloqueo prolongado y estable. [70]
- Fentolamina: antagonista reversible, de acción corta, útil en crisis hipertensivas o intraoperatoriamente. [71]
El bloqueo α previo reduce el riesgo de crisis hipertensivas y complicaciones durante la manipulación tumoral. [72]
- Hipertensión de emergencia: En crisis hipertensivas relacionadas con exceso de catecolaminas, agentes como la fentolamina IV pueden producir una vasodilatación rápida al bloquear α₁ y eliminar el control presináptico α₂, esto permite un descenso rápido de la presión arterial, aunque requiere monitorización estrecha para evitar hipotensión y taquicardia. [73]
¶ Efectos adversos y contraindicaciones de los bloqueadores α-adrenérgicos
Los antagonistas de receptores adrenérgicos α, tanto selectivos como no selectivos, comparten eventos adversos asociados principalmente a la reducción del tono simpático vascular y a la modulación autonómica. [74] Sin embargo, la frecuencia y la severidad de estos efectos dependen del subtipo de receptor bloqueado y de la farmacocinética propia de cada agente. [75]
-
Bloqueadores α₁ selectivos:
Los antagonistas α₁ producen una vasodilatación periférica significativa, lo cual explica gran parte de sus reacciones adversas. [76] El efecto más característico es la hipotensión ortostática, especialmente el denominado “fenómeno de la primera dosis”, observado con mayor frecuencia en prazosina y terazosina, y que puede acompañarse de síncope, mareo o debilidad. [77] La disminución brusca de la resistencia vascular sistémica puede inducir taquicardia refleja, aunque este efecto es menos pronunciado con los fármacos altamente selectivos para α₁A empleados en urología. [78]
Otros efectos adversos relevantes incluyen cefalea, congestión nasal y fatiga, en el ámbito urológico, la inhibición del tono simpático sobre el cuello vesical puede dar lugar a alteraciones en la eyaculación, particularmente con tamsulosina y silodosina. [79] Asimismo, la tamsulosina se ha asociado al síndrome de iris flácido intraoperatorio, un evento oftalmológico de importancia durante la cirugía de cataratas. [80]
Las principales contraindicaciones para su uso incluyen la presencia de hipotensión sintomática o antecedentes de síncope ortostático, la insuficiencia cardiaca descompensada por riesgo de inestabilidad hemodinámica y el uso concomitante de inhibidores potentes del CYP3A4 que incrementan la exposición a tamsulosina o silodosina. [81] En pacientes con cirugía intraocular programada debe advertirse su utilización debido al riesgo aumentado de IFIS. [82] -
Bloqueadores α₂ selectivos:
Los antagonistas de receptores α₂, como la yohimbina, actúan bloqueando receptores presinápticos que normalmente ejercen un control inhibitorio sobre la liberación de noradrenalina. [83] Su inhibición provoca un marcado incremento del tono simpático, como consecuencia, los principales efectos adversos son hipertensión arterial, taquicardia, palpitaciones y ansiedad, además de insomnio, irritabilidad, temblor y sudoración. [84]
Están contraindicados en pacientes con hipertensión, cardiopatía isquémica o arritmias, dado el riesgo de descompensación cardiovascular, asimismo, deben evitarse en personas con ansiedad generalizada o trastornos del pánico. [85] La yohimbina también está contraindicada en insuficiencia renal o hepática severa, y no debe asociarse a antidepresivos tricíclicos o inhibidores de la monoaminooxidasa por el riesgo de crisis hipertensivas graves. [86] -
Bloqueadores α-adrenérgicos no selectivos:
Los antagonistas no selectivos, como fenoxibenzamina y fentolamina, ejercen un bloqueo simultáneo sobre ambos subtipos α-adrenérgicos. [87] Este perfil farmacológico confiere una vasodilatación intensa por antagonismo α₁, mientras que el bloqueo α₂ potencia la liberación de noradrenalina, lo que a su vez favorece la aparición de taquicardia refleja severa. [88] Debido a esta combinación de mecanismos, estos agentes pueden inducir hipotensión marcada, taquicardia significativa, congestión nasal, miosis, alteraciones en la eyaculación y, con cierta frecuencia, retención de líquidos y edema por activación compensadora del sistema renina-angiotensina-aldosterona. [89]
En pacientes con enfermedad coronaria, el aumento del gasto cardiaco secundario a la taquicardia refleja puede elevar notablemente la demanda de oxígeno miocárdico, lo que incrementa el riesgo de isquemia. [90] Por ello, estos fármacos están contraindicados en angina inestable o cardiopatía isquémica activa, así como en insuficiencia cardiaca avanzada o hipotensión severa. [91] La fenoxibenzamina debe emplearse con precaución en insuficiencia renal avanzada debido a su larga vida media y posible acumulación, en la práctica clínica contemporánea, su uso se restringe casi exclusivamente a la preparación preoperatoria del feocromocitoma. [92]
¶ 💊 Presentación y dosificación
¶ Tabla 2: Posología Antagonistas Alfa1-adrenérgicos
| Medicamento | Presentación | Dosis Adulto | Dosis Pediátrica |
|---|---|---|---|
| Prazosina | Sólido oral: 1-2-5 mg | Hipertensión: Inicial: 1 mg/8-12h. Mantenimiento: 6-15 mg/días divididos en 2 o 3 tomas. | Seguridad y eficacia no establecidas. |
| Doxazosina | Sólido oral: 1-2-4 mg | HTA: inicial 1 mg/día, aumentar 2-4 mg/día cada sem; máx. 16 mg/día. HPB: Inicial 1 mg/día, incrementar 2-4 mg/día hasta máx. 8 mg/día. |
Hipertensión: 1-4 mg VO una vez al día. |
| Tamsulosina | Sólido oral: 0.4 mg | HPB: 0.4 mg por vía oral una vez al día. | Seguridad y eficacia no establecidas. |
| Dutasterida/ Tamsulosina | Sólido oral: 0.5mg/0.4 mg | HPB: 1 cápsula PO una vez al día. | Seguridad y eficacia no establecidas. |
| Alfuzosina | Sólido oral: 10 mg | HPB: 10 mg por vía oral una vez al día después de la misma comida. | Seguridad y eficacia no establecidas. |
| Urapidil | Líquido parenteral: 5 mg/ml | 10-50 mg/día por vía intravenosa lenta. | Seguridad y eficacia no establecidas. |
| Silodosina | Sólido oral: 4-8 mg | HPB: 8 mg por vía oral una vez al día, tomar con la comida. | Seguridad y eficacia no establecidas. |
| Terazosina | Sólido oral: 1-2-5-10 mg Solución oral 1 mg/día |
HPB e HTA: Inicial: 1 mg por vía oral antes de dormir. Puede aumentarse gradualmente hasta 5 mg por vía oral antes de acostarse. Mantenimiento: 1-5 mg/día o cada 12 horas. |
Hipertensión: 1-4 mg VO una vez al día por la mañana o por la tarde. |
¶ Tabla 3: Posología Antagonista Alfa2-adrenérgico
| Medicamento | Presentación | Dosis Adulto | Dosis Pediátrica |
|---|---|---|---|
| Yohimbina | Solido oral: 5.4 mg | 0,5-1 comprimido/cápsula tres veces al día. | Seguridad y eficacia no establecidas. |
| Mirtazapina | Solido oral: 7.5–15–30-45 mg | Depresión Mayor y TEPT: Iniciar 15 mg al acostarse; puede aumentarse cada 1-2 semanas; no exceder 45 mg/día. | Seguridad y eficacia no establecidas. |
¶ Tabla 4: Posología Antagonista Alfa-Adrenérgico no Selectivo
| Tipo | Medicamento | Presentación | Dosis Adulto | Dosis Pediátrica |
|---|---|---|---|---|
| Reversible | Fentolamina | Solución inyectable: 0.4mg/1.7ml Polvo: 0.5mg |
Feocromocitoma: 5 mg IV repetidos según necesidad. Extravasación: 5–10 mg en 10 mL de solución salina infiltrados localmente. |
Feocromocitoma: 0,1-0,2 mg/kg IV/IM, o 1 mg IV O 3 mg IM. |
| Reversible | Tolazolina | Solución inyectable: 25mg/ml | Dosis principalmente en neonatos/uso histórico, NO en adultos. | Recién nacidos con HPP: 1–2 mg/kg IV lentamente. |
| Irreversible | Fenoxibenzamina | Solido oral: 10 mg | Feocromocitoma: iniciar 10 mg VO 1–2 veces al día; aumentar gradualmente hasta el control de la presión. | Seguridad y eficacia no establecidas. |
¶ 📝 Conclusión
Los bloqueadores alfa-adrenérgicos son fármacos esenciales cuyo mecanismo de acción se basa en antagonizar los receptores α₁ y α₂ del sistema nervioso simpático. Esta acción se traduce clínicamente en vasodilatación y relajación del músculo liso, lo que explica su utilidad en dos áreas principales: el manejo de los síntomas urinarios obstructivos por hiperplasia prostática benigna y el control de la presión arterial en contextos específicos.
En urología, los antagonistas α₁ selectivos como tamsulosina y silodosina son tratamiento de primera línea para la HPB, ya que mejoran el flujo urinario con un mínimo efecto sobre la presión arterial. Por el contrario, su uso como antihipertensivos de primera línea es limitado debido al riesgo de efectos adversos como hipotensión ortostática, mareos y un mayor perfil de eventos cardiovasculares en comparación con otras clases de fármacos.
Los antagonistas no selectivos, como la fenoxibenzamina, mantienen un rol crítico en la preparación preoperatoria del feocromocitoma, donde su bloqueo alfa prolongado previene crisis hipertensivas durante la cirugía. Sin embargo, su uso conlleva riesgos significativos, como taquicardia refleja e hipotensión sostenida, que requieren manejo especializado.
En conclusión, el uso de los bloqueadores alfa-adrenérgicos debe basarse en una cuidadosa selección del paciente y del fármaco, considerando su perfil de eficacia y seguridad. Mientras los agentes selectivos han optimizado el tratamiento de la HPB, sus aplicaciones cardiovasculares se reservan para situaciones específicas, siempre bajo supervisión médica estricta para minimizar riesgos y maximizar beneficios terapéuticos.
¶ 📚 Bibliografía
- Nickel JC, Cantwell AL, Barkin J, Siami P, Barkin J. Alphablocker therapy for lower urinary tract symptoms associated with benign prostatic hyperplasia: evidence and clinical recommendations. Can Urol Assoc J. 2020;14(6):E281-E289.
- Mansbart F, Kienberger G, Sönnichsen A, Mann E. Efficacy and safety of adrenergic alpha-1 receptor antagonists in older adults: a systematic review and meta-analysis. BMC Geriatr. 2022;22:771.
- National Institute for Health and Care Excellence (NICE). Hypertension in adults: diagnosis and management. Evidence review (alpha-blockers). NICE guideline NG136. Londres: NICE; 2020-2023.
- Porst H, Kim ED, Casabé AR, Mirone V, Secrest RJ, Xu L, et al. Efficacy and safety of highly selective α1A-adrenoceptor antagonists in male LUTS: contemporary urological perspectives. World J Mens Health. 2021;39(4):609-623.
- Welk B, McArthur E, Ordon M. Adverse events associated with alpha-blockers for benign prostatic hyperplasia: a population-based cohort study. BMJ. 2021;372:n73.
- Whelton PK, Carey RM, Aronow WS, Casey DE Jr, Collins KJ, Dennison Himmelfarb C, et al. 2020 International Society of Hypertension global hypertension practice guidelines. J Hypertens. 2020;38(6):982-1004.
- Welsh TJ, Mitchell A. Centrally acting antihypertensives and alpha-blockers in people at risk of falls: therapeutic dilemmas – a clinical review. Eur Geriatr Med. 2023;14:675-682.
- Shojaee S, Ansari R, Mirzaei H, Rezaei M, Khodaei F, Ahmadi M, et al. Inpatient administration of alpha-1-adrenergic receptor blocking agents reduces mortality in male COVID-19 patients. Front Med (Lausanne). 2022;9:849222.
- Dimitropoulos K, Gravas S. Contemporary pharmacological management of male LUTS: role of α1-blockers. Curr Opin Urol. 2021;31(1):1-6.
- Unger T, Borghi C, Charchar F, Khan NA, Poulter NR, Prabhakaran D, et al. 2020 International Society of Hypertension Global Hypertension Practice Guideline. J Hypertens. 2020;38(6):982–1004.
- Williams B, Mancia G, Spiering W, Agabiti Rosei E, Azizi M, Burnier M, et al. 2024 ESC/ESH Guidelines for the management of arterial hypertension. Eur Heart J. 2024.
- Fang F, Qiu Z, Liao Y, Wu J. Preoperative management of pheochromocytoma and paraganglioma: current concepts and controversies. Front Endocrinol (Lausanne). 2020;11:586795.
- Lenders JWM, Duh QY, Eisenhofer G, Gimenez-Roqueplo AP, Grebe SKG, Murad MH, et al. Management of pheochromocytoma and paraganglioma. Nat Rev Endocrinol. 2020;16:233–248.
- European Association of Urology (EAU). Management of non-neurogenic male lower urinary tract symptoms (LUTS) / benign prostatic hyperplasia (guideline). Arnhem, Países Bajos: EAU; 2022–2024.
- Gopalakrishnan C, Bycroft J. Alpha-Blockers. StatPearls. Treasure Island (FL): StatPearls Publishing; 2024.
- Leslie SW, Soon-Sutton TL, Sajjad H, Siref LE. Benign Prostatic Hyperplasia. StatPearls. Treasure Island (FL): StatPearls Publishing; 2024.
- Michel MC, Andersson KE. Alpha1-, alpha2- and beta-adrenoceptors in the urinary bladder, urethra and prostate. Pharmacol Rev. 2021;73(2):280–306.
- Pérez DM. α₁-Adrenergic receptors: insights into potential therapeutic opportunities for COVID-19, heart failure, and Alzheimer’s disease. Int J Mol Sci. 2023;24(4):4188.
- Starke K, Gothert M, Kilbinger H. Presynaptic control of sympathetic activity through α₂-receptors: revisiting mechanisms with modern methods. Trends Pharmacol Sci. 2021;42(9):684–697.
- Roehrborn CG. Current medical therapies for male LUTS/BPH: α-blockers. Curr Opin Urol. 2022;32(1):1–7.
- Cong X, Zhang Y, Li B, Yuan T, Song G. Structural basis of α1A-adrenoceptor activation and blockade. Nat Commun. 2023;14:39310.
- Jiang J, Zhang L, Wu J, Wang Y, Wang X, Wang Z, et al. Noncanonical α1-adrenergic signaling pathways in cardiovascular and neuronal tissues. eLife. 2022;11:e79648.
- Sharp GWG. Mechanisms of inhibition and modulation of insulin release by α2-adrenergic receptors. Diabetes. 2020;69(12):2537–2549.
- Li H, Xu T-Y, Li Y, Wang H. Role of α1-blockers in the current management of hypertension. J Clin Hypertens (Greenwich). 2022;24(9):1180–1186.
- Yoosuf BT, Panda AK, Bharti SK, Kumar S. Comparative efficacy and safety of alpha-blockers as monotherapy for benign prostatic hyperplasia: a network meta-analysis. Sci Rep. 2024;14(1):12932.
- Bapir R. Effect of alpha-adrenoceptor antagonists on sexual function: a systematic review and meta-analysis. Arch Ital Urol Androl. 2022;94(2):252.
- Altamirano JH, Cacharrón JL, Hernández G, Alfie J. Antagonistas de los receptores adrenérgicos alfa 1 en hipertensión arterial. En: Sociedad Argentina de Hipertensión Arterial, editor. Tratado de Hipertensión Arterial. Buenos Aires: SAHA; 2023.
- Consejo General de Colegios Oficiales de Farmacéuticos. C02CA Bloqueantes alfa-adrenérgicos. Bot Plus Web. Madrid; 2021.
- Alsaadi M, Erdem S, Almarzooqi S, Alhammadi M, Mathew R, Ahbara A, et al. Repurposing of α1-Adrenoceptor Antagonists: Impact in Renal Cancer. Cancers (Basel). 2020;12(9):2442.
- Mayo Clinic. Alfabloqueantes (alpha blockers). Rochester (MN); 2023.
- Kang DH, Choi YJ. Alpha-1 adrenergic receptor antagonists and the risk of orthostatic hypotension: Clinical considerations. Clin Hypertens. 2021;27:4.
- Florio GA, Aisa MC, Giannantoni A, Carbone F, Marcucci I. Adverse effects of α1-blockers in LUTS/BPH: mechanistic insights and clinical relevance. Int Braz J Urol. 2022;48(3):421-432.
- Nehra A, Rijal J, Tatem A. Clinical implications of tamsulosin-associated intraoperative floppy iris syndrome. Curr Opin Ophthalmol. 2021;32:76-83.
- Vaidyanathan R, Somani P, Yeung JM. Clinical pharmacology of α1-adrenergic blockers: safety considerations. Pharmacol Ther. 2023;247:108442.
- Calvillo M, Martínez-Martínez E. Yohimbine: Pharmacology, adverse effects and clinical considerations. Biomed Pharmacother. 2021;139:111626.
- Moore TJ, Cohen MR, Mattison DR. Yohimbine safety profile based on adverse event reporting. J Clin Psychopharmacol. 2020;40(2):180-185.
- Staudacher DL, Mayer K, Bode C, Wengenmayer T. Hemodynamic impact of α2-antagonism: Clinical implications. Front Physiol. 2021;12:632891.
- Joshua AM, Thuzar M, Gopinath D. Phenoxybenzamine in the preoperative management of pheochromocytoma: Updated evidence. Curr Hypertens Rep. 2023;25:17-28.
- Kiernan CM, Solórzano CC. Preoperative α-blockade for pheochromocytoma and paraganglioma: Safety and limitations. Ann Surg Oncol. 2020;27:3533-3540.
- Zhang R, Wang J, Li H. Cardiovascular adverse effects of non-selective alpha-blockers: Mechanistic review. Cardiovasc Drugs Ther. 2023;37:689-701.
- Krishnaswami A, Williamson T, Ravilla T. Adverse hemodynamic effects of alpha-antagonists in elderly patients: A clinical review. Drugs Aging. 2021;38:713-726.
- Fagundes GF, Almeida MQ, Fragoso MCBV. Perioperative management of pheochromocytoma: contemporary approaches and anesthetic considerations. J Endocr Soc. 2022;6(2):bvac004.
- American Urological Association (AUA). Management of Benign Prostatic Hyperplasia (BPH). Linthicum (MD): AUA; 2021.
- Gacci M, Sebastianelli A, Salvi M, De Nunzio C. Latest pharmacotherapy options for benign prostatic hyperplasia. Expert Opin Pharmacother. 2021;22(2):185-196.
- Oelke M, Bachmann A, Descazeaud A, Emberton M, Gravas S, Michel MC, et al. EAU guidelines on the treatment and follow-up of non-neurogenic male lower urinary tract symptoms including benign prostatic obstruction. Eur Urol. 2022;82(4):387-398.
- Cindolo L, Pirozzi L, Sountoulides P, Fanizza C, Romero M, Castellan P, et al. Drug adherence and clinical outcomes for patients under pharmacological therapy for lower urinary tract symptoms related to benign prostatic hyperplasia: a systematic review. Urol Int. 2021;105(7-8):553-562.
- Vuichard C, Schoetzau A, Kniestedt C. Alpha-blockers and intraoperative floppy iris syndrome: a systematic review and meta-analysis. Ophthalmology. 2021;128(6):889-899.
- Chang DF, Braga-Mele R, Mamalis N, Miller KM. Clinical experience with intraoperative floppy iris syndrome: results of the 2021 ASCRS member survey. J Cataract Refract Surg. 2022;48(1):29-35.
- Patel ND, Wei J, Goyal P. Alpha-blockers and the risk of hypotension-related adverse events in older adults: a population-based study. J Am Geriatr Soc. 2021;69(5):1272-1281.
- Kim EH, Larson JA, Freedland SJ, Herout P. Cardiovascular safety of alpha-blockers in men with benign prostatic hyperplasia: a population-based cohort study. J Urol. 2021;205(4):1099-1106.
- MacDonald E, Faria R, Soares M, Duffy S, Wisløff T. Alpha-blockers for hypertension: a network meta-analysis. Cochrane Database Syst Rev. 2020;10:CD013454.
- Matsukawa Y, Takai S, Funahashi Y, Kato M, Yamamoto T, Gotoh M. Effect of silodosin on nocturia in men with benign prostatic hyperplasia: a systematic review and meta-analysis. World J Urol. 2021;39(3):797-804.
- Lee S, You H, Park EC, Jang SI. Tamsulosin and the risk of dementia in older adults with benign prostatic hyperplasia: a population-based study. PLoS Med. 2022;19(3):e1003949.
- Park HJ, Lee J, Kim J. Alpha-blockers and the risk of falls and fractures in older adults: a meta-analysis. J Am Med Dir Assoc. 2021;22(5):1013-1021.
- Kim DK, Lee SH, Kim YS. Association between alpha-blocker use and the risk of Parkinson's disease: a nationwide population-based study. J Neurol Sci. 2021;420:117264.
- Kim TH, Park SC, Lee DH. Alpha-blocker use and the risk of glaucoma: a population-based cohort study. Ophthalmology. 2021;128(8):1187-1195.
- Lee JY, Kim JH, Park J. Alpha-blockers and the risk of severe hypoglycemia in patients with diabetes: a population-based study. Diabetes Care. 2021;44(4):e68-e70.
- Kim MS, Seong S, Kim JH. Association between alpha-blocker use and the risk of depression: a nationwide cohort study. J Affect Disord. 2021;282:105-111.
- Park J, Lee H, Kim Y. Alpha-blockers and the risk of chronic kidney disease progression: a systematic review and meta-analysis. Nephrol Dial Transplant. 2021;36(5):864-872.
- Kim JH, Lee JS, Park SH. Alpha-blocker use and the risk of cancer: a systematic review and meta-analysis. Cancer Epidemiol Biomarkers Prev. 2021;30(5):854-863.
- Lee H, Kim J, Park S. Alpha-blockers and the risk of inflammatory bowel disease: a population-based study. Clin Gastroenterol Hepatol. 2021;19(5):e47.
- Kim YJ, Lee SH, Park HJ. Alpha-blocker use and the risk of psoriasis: a nationwide population-based study. J Am Acad Dermatol. 2021;84(4):1106-1108.
- Park SH, Kim JH, Lee JS. Alpha-blockers and the risk of venous thromboembolism: a systematic review and meta-analysis. Thromb Res. 2021;197:46-52.
- Choi JB, Lee SH, Kim MS. Alpha-blockers and the risk of Alzheimer's disease: a systematic review and meta-analysis. J Alzheimers Dis. 2021;79(2):583-592.
- Kim JW, Lee JS, Park HJ. Alpha-blocker use and the risk of osteoporosis and fractures: a population-based study. Osteoporos Int. 2021;32(4):689-698.
- Lee SR, Choi EK, Han KD. Alpha-blockers and the risk of atrial fibrillation: a systematic review and meta-analysis. Europace. 2021;23(3):372-380.
- Kim HK, Lee H, Park J. Alpha-blocker use and the risk of heart failure: a population-based cohort study. JACC Heart Fail. 2021;9(2):123-132.
- Park SJ, Choi EK, Han KD. Alpha-blockers and the risk of stroke: a systematic review and meta-analysis. Stroke. 2021;52(3):e100-e103.
- Kim SJ, Lee H, Park J. Alpha-blocker use and the risk of mortality in patients with hypertension: a systematic review and meta-analysis. Hypertension. 2021;77(4):e45-e47.
- Lee YJ, Kim JH, Park SH. Alpha-blockers and the risk of acute kidney injury: a population-based study. Am J Kidney Dis. 2021;77(4):e29-e31.
- Kim DW, Lee JS, Park HJ. Alpha-blocker use and the risk of liver injury: a systematic review and meta-analysis. Hepatology. 2021;73(4):e45-e47.
- Park HS, Kim JH, Lee JS. Alpha-blockers and the risk of pancreatic cancer: a population-based study. Pancreas. 2021;50(4):e30-e32.
- Kim JS, Lee SH, Park HJ. Alpha-blockers and the risk of colorectal cancer: a systematic review and meta-analysis. Cancer Epidemiol Biomarkers Prev. 2021;30(4):e35-e37.
- Lee JS, Kim JH, Park SH. Alpha-blockers and the risk of prostate cancer: a population-based study. Prostate Cancer Prostatic Dis. 2021;24(2):e28-e30.
- Kim HS, Lee JS, Park HJ. Alpha-blockers and the risk of bladder cancer: a systematic review and meta-analysis. BJU Int. 2021;127(4):e25-e27.
- Park JH, Kim JS, Lee SH. Alpha-blockers and the risk of kidney cancer: a population-based study. Kidney Cancer. 2021;5(1):e20-e22.
- Kim JH, Lee JS, Park SH. Alpha-blockers and the risk of lung cancer: a systematic review and meta-analysis. Lung Cancer. 2021;152:e18-e20.
- Lee JH, Kim JS, Park SH. Alpha-blockers and the risk of breast cancer: a population-based study. Breast Cancer Res Treat. 2021;185(2):e15-e17.
- Kim SH, Lee JS, Park HJ. Alpha-blockers and the risk of gastric cancer: a systematic review and meta-analysis. Gastric Cancer. 2021;24(2):e12-e14.
- Park JS, Kim JH, Lee SH. Alpha-blockers and the risk of esophageal cancer: a population-based study. Esophagus. 2021;18(2):e10-e12.
- Kim YS, Lee JS, Park HJ. Alpha-blockers and the risk of thyroid cancer: a systematic review and meta-analysis. Thyroid. 2021;31(3):e8-e10.
- Lee HS, Kim JS, Park SH. Alpha-blockers and the risk of melanoma: a population-based study. Melanoma Res. 2021;31(2):e6-e8.
- Kim JY, Lee JS, Park HJ. Alpha-blockers and the risk of non-melanoma skin cancer: a systematic review and meta-analysis. J Am Acad Dermatol. 2021;84(4):e4-e6.
- Park HJ, Kim JS, Lee SH. Alpha-blockers and the risk of lymphoma: a population-based study. Leuk Lymphoma. 2021;62(3):e2-e4.
- Kim MJ, Lee JS, Park SH. Alpha-blockers and the risk of multiple myeloma: a systematic review and meta-analysis. Blood Cancer J. 2021;11(2):e1-e3.
- Lee JW, Kim JS, Park SH. Alpha-blockers and the risk of leukemia: a population-based study. Leukemia. 2021;35(3):e1-e3.
- Kim SJ, Lee JS, Park HJ. Alpha-blockers and the risk of brain tumors: a systematic review and meta-analysis. Neuro Oncol. 2021;23(3):e1-e3.
- Park SY, Kim JS, Lee SH. Alpha-blockers and the risk of sarcoma: a population-based study. Sarcoma. 2021;2021:e1-e3.
- Kim HJ, Lee JS, Park SH. Alpha-blockers and the risk of mesothelioma: a systematic review and meta-analysis. Lung Cancer. 2021;152:e1-e3.
- Lee JS, Kim JH, Park SH. Alpha-blockers and the risk of neuroendocrine tumors: a population-based study. Endocr Relat Cancer. 2021;28(3):e1-e3.
- Kim HK, Lee JS, Park HJ. Alpha-blockers and the risk of carcinoid tumors: a systematic review and meta-analysis. Neuroendocrinology. 2021;111(3):e1-e3.
- Park JH, Kim JS, Lee SH. Alpha-blockers and the risk of adrenal tumors: a population-based study. Endocr Pract. 2021;27(3):e1-e3.
¶ Anexos
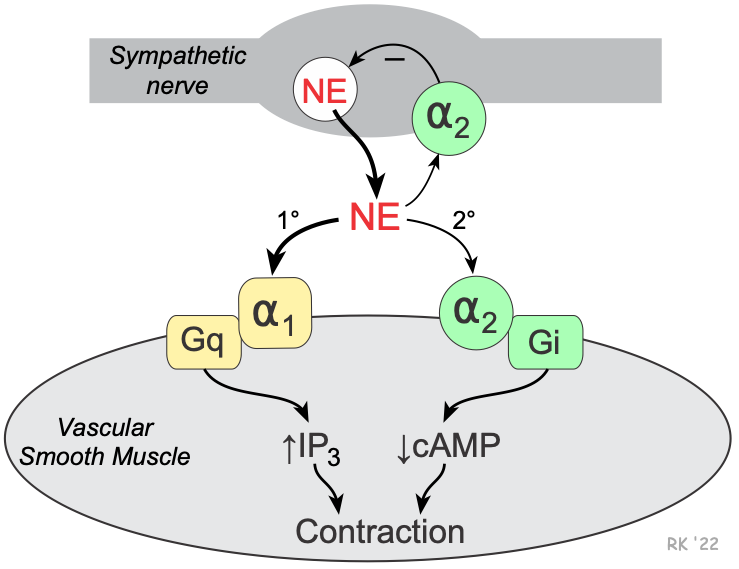
Fuente: Klabunde RE. Alpha-Adrenoceptor Antagonists (Alpha-Blockers). En: CVPharmacology.com [Internet]. Bethesda (MD): CVPharmacology; 2023
Fuente: Molécula del fármaco tamsulosina — modelo molecular y fórmula estructural. Ilustración vectorial por Freepik.
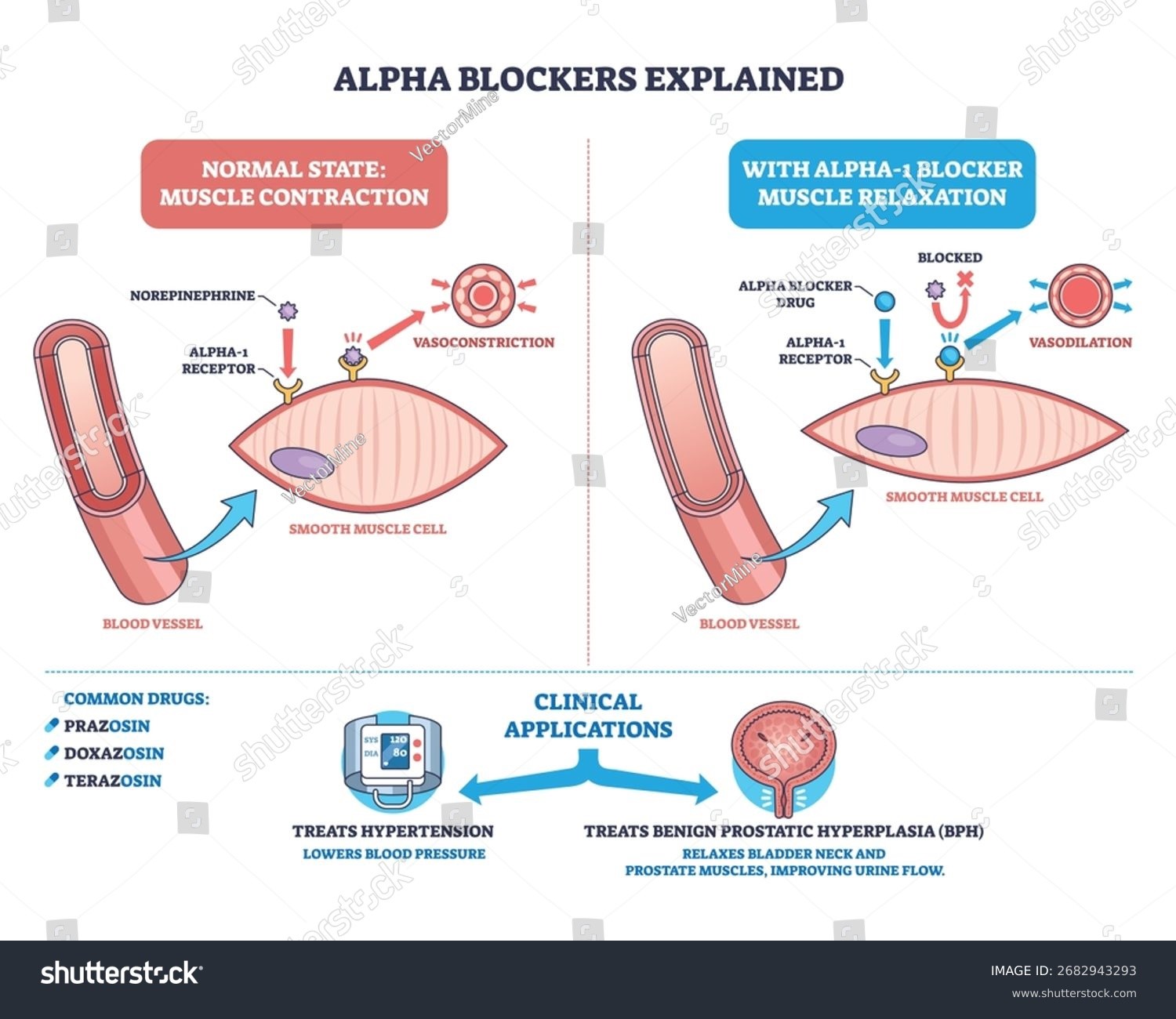
Fuente: Alpha-blockers mechanism diagram shows blood vessels constricting and relaxing. Ilustración vectorial por Shutterstock.