¶ INTRODUCCIÓN
Clasificar a las bacterias en Gram positivas y Gram negativas según su comportamiento frente a la tinción de Gram es fundamental en microbiología clínica ya que esta categorización no solo tiene utilidad diagnóstica sino también profundas implicaciones terapéuticas porque la estructura de la pared celular determina su susceptibilidad a distintos antibióticos lo que hace que comprender estas diferencias sea crucial para una selección empírica adecuada del tratamiento especialmente en situaciones sin un antibiograma inmediato.1
La pared celular de las bacterias Gram positivas está compuesta por una gruesa capa de peptidoglicano, lo que las hace más susceptibles a antibióticos que inhiben la síntesis de la pared celular, como los β-lactámicos y los glicopéptidos, por el contrario, las bacterias Gram negativas poseen una membrana externa rica en lipopolisacáridos (LPS), que actúa como una barrera física frente a muchos antibióticos, confiriéndoles una resistencia intrínseca mayor y requiriendo el uso de moléculas capaces de atravesar dicha membrana, como las fluoroquinolonas o los aminoglucósidos.2
A continuación, presentamos las principales diferencias entre una bacteria Gram positiva y Gram negativa que debemos tener en cuenta para la correcta selección del fármaco en su uso empírico:
Tabla 1: Diferencias entre Bacterias Gram positivas y Gram negativas.
| Característica | Gram Positivas | Gram Negativas |
|---|---|---|
| Tinción de Gram | Retienen el cristal violeta (color morado) | Se tiñen con safranina (color rosado/rojo) |
| Pared celular | Gruesa capa de peptidoglicano (hasta el 90%) | Delgada capa de peptidoglicano |
| Membrana externa | Ausente | Presente, rica en lipopolisacáridos (LPS) |
| Espacio periplásmico | Mínimo o ausente | Presente, entre membrana externa y membrana plasmática |
| Ácidos teicoicos/ lipoteicoicos | Presentes, aportan rigidez y adhesión | Ausentes |
| Lipopolisacáridos (LPS) | Ausentes | Presentes, actúan como endotoxina |
| Sensibilidad a antibióticos | Mayor sensibilidad a β-lactámicos y glicopéptidos | Más resistente a ciertos antibióticos por barrera externa |
Tabla creada por autores
La diferenciación entre bacterias Gram positivas y negativas posee un gran valor clínico al influir directamente en el enfoque terapéutico y en la comprensión de la evolución de la infección, las bacterias Gram negativas al liberar LPS pueden provocar estados clínicos graves como el shock séptico debido a la activación de una respuesta inflamatoria sistémica severa, por su parte las Gram positivas aunque carecen de LPS pueden producir exotoxinas potentes como las de Staphylococcus aureus o Clostridioides difficile que causan cuadros clínicos igualmente críticos.3
Las infecciones nosocomiales por bacterias Gram negativas multirresistentes como Pseudomonas aeruginosa, Acinetobacter baumannii y Klebsiella pneumoniae representan un desafío terapéutico en hospitales debido a su limitada sensibilidad a antibióticos convencionales, paralelamente los Gram positivos como Staphylococcus aureus resistente a meticilina (MRSA) o Enterococcus faecium resistente a vancomicina (VARS) requieren terapias dirigidas y vigilancia estricta la correcta clasificación de los agentes causales permite optimizar el tratamiento empírico minimizar resistencias y mejorar el pronóstico del paciente.4
La selección adecuada de antibióticos basada en la clasificación Gram y la susceptibilidad específica del patógeno es crucial para el tratamiento efectivo de infecciones bacterianas y para combatir la resistencia antimicrobiana, por tal motivo comprender tanto las estructurales y funcionales entre bacterias Gram positivas y negativas junto con el conocimiento de las opciones terapéuticas disponibles permite a los profesionales sanitarios tomar decisiones informadas y mejorar los resultados clínicos.5
Dianas de actuación de los antimicrobianos en bacterias Gram Positivas y Gram Negativas.
Los antibióticos ejercen su acción sobre estructuras y procesos bacterianos esenciales, a continuación, se describen las principales dianas terapéuticas:
Inhibición de la síntesis de la pared celular.
Inhibición de la síntesis del peptidoglicano (etapas tempranas y precursores):
- Fosfomicina: Inhibe de forma irreversible la enzima MurA (UDP-N-acetilglucosamina enolpiruvil transferasa), que cataliza el primer paso de la síntesis del peptidoglicano, este grupo tiene un amplio espectro de actividad.6
- Cicloserina: Es un análogo estructural de la D-alanina que inhibe dos enzimas cruciales, la Alanina racimasa y D-Alanina-D-Alanina ligasa, involucradas en la formación del dipéptido precursor del peptidoglicano, este se reserva para infecciones graves como la tuberculosis.6
- Inhibición del transporte de precursores y polimerización (etapa intermedia):
- Bacitracina: Bloquea la desfosforilación del transportador lipídico, que es esencial para llevar los precursores del peptidoglicano a través de la membrana celular, al agotarse este transportador, la síntesis se detiene, estos fármacos son principalmente efectiva contra bacterias Gram positivas.7
- Inhibición de la transglicosilación y reticulación (etapa final):
- β-lactámicos: Inhiben la síntesis del peptidoglicano al unirse irreversiblemente a las enzimas Penicilina Binding Proteins, que son responsables de la transglicosilación y la transpeptidación, son muy efectivos contra Gram positivas.6
- Glucopéptidos: Se unen con alta afinidad al sustrato D-Ala-D-Ala de los precursores del peptidoglicano, esto impide físicamente que las PBPs realicen la reacción de transpeptidación, estas son moléculas grandes que no atraviesan fácilmente la membrana externa de Gram negativas.7
- Tunicamicina: Es una molécula experimental que inhibe la enzima MraY, evitando la formación del primer complejo lipídico precursor en la síntesis del peptidoglicano, sin embargo, también inhibe enzimas similares en células eucariotas, por lo que es demasiado tóxica para su uso clínico en humanos, este se utiliza principalmente en investigación.6
Inhibición de la síntesis de proteínas.
Aminoglucósidos: inhiben la subunidad 30S ribosomal. Muy eficaces en Gram negativas.8
- Macrólidos: inhiben la subunidad 50S, más usados en Gram positivas y atípicos.
- Tetraciclinas: afectan la subunidad 30S, tienen espectro amplio.8
Inhibición de la síntesis de ácidos nucleicos.
Inhibición de la replicación del ADN.
- Quinolonas: Inhiben la ADN girasa en bacterias Gram negativas y la topoisomerasa IV en Gram positivas, esto impide la relajación del superenrollamiento del ADN, deteniendo la replicación y la transcripción. 9
- Inhibición de la transcripción.
- Rifampicina: Se une de forma específica e irreversible a la subunidad beta de la ARN polimerasa dependiente de ADN bacteriana, bloqueando la iniciación de la transcripción, es especialmente eficaz contra Mycobacterium tuberculosis y algunas bacterias Gram positivas. 9
- Actinomicina D: Este compuesto también inhibe la transcripción al unirse al ADN e intercalarse en él, impidiendo el avance de la ARN polimerasa, sin embargo, no es selectiva y actúa tanto en células procariotas como eucariotas, por lo que es demasiado tóxica para su uso como antibacteriano. 9
- Inhibición de la replicación tras dañar el ADN.
- Nitroimidazoles: Son profármacos que se activan de forma selectiva en bacterias anaerobias y protozoos, una vez activados, forman radicales libres que causan rupturas en las hebras de ADN y su posterior degradación.9
Inhibición de la síntesis de Metabolitos esenciales como el ácido fólico.
- Trimetroprin-sulfametoxazol: inhibe pasos secuenciales en la síntesis del ácido fólico bacteriano, siendo un antibiótico de amplio espectro amplio.10
Alteración de la función de la membrana citoplasmática.
Polimixinas: Se unen a los lipopolisacáridos de la membrana externa de las bacterias Gram negativas, desplazando los iones Ca²⁺ y Mg²⁺ que la estabilizan, esto altera su permeabilidad.10
- Daptomicina: Perfora y despolariza la membrana de bacterias Gram positivas.
- Lipopéptidos: No atacan la membrana directamente, sino que inhiben la síntesis de la pared celular de los hongos.8
- Azoles: No rompen la membrana, sino que inhiben la síntesis del ergosterol, el componente clave que la forma y estabiliza.8
¶ DESARROLLO.
¶ GRAM POSITIVAS.
Las bacterias Gram positivas poseen una gruesa capa de peptidoglicano en su pared celular que retiene el color violeta durante la tinción de Gram. Carecen de membrana externa, lo que facilita la acción de los antibióticos β lactámicos y glucopéptidos, sin embargo, la aparición de mecanismos de resistencia como modificación de las proteínas ligadoras de penicilina (PBPs), bombas de eflujo y alteraciones en la permeabilidad de la pared ha aumentado en los últimos años, alcanzando hasta un 10–15 % de aislados de Streptococcus pneumoniae con resistencia intermedia en Europa y América desde 2020 11
-
¶ No productoras de β-Lactamasa.
Las bacterias Gram positivas no productoras de β lactamasa carecen de enzimas que inactiven los antibióticos β lactámicos, lo que suele traducirse en una alta susceptibilidad a este grupo, no obstante, existe un riesgo creciente de resistencia mediada por la modificación de las proteínas ligadoras de penicilina (PBPs), bombas de eflujo y cambios en la permeabilidad de la pared celular, fenómenos que han sido documentados en hasta un 10 15 % de aislamientos de Streptococcus pneumoniae en algunos estudios recientes, por ello, es esencial monitorizar continuamente los perfiles de sensibilidad local y ajustar la dosificación de los β lactámicos según parámetros de farmacocinética y farmacodinamia para asegurar niveles terapéuticos óptimos en el sitio de la infección y prevenir el desarrollo de resistencia.12
Principales Patógenos.
- Streptococcus pyogenes (grupo A): responsable de faringitis, impétigo y fascitis necrotizante; mantiene > 95 % de sensibilidad a penicilina.13
- Streptococcus pneumoniae: causa frecuente de neumonía adquirida en la comunidad y otitis media.13
- Enterococcus faecalis sensible: implicado en infecciones del tracto urinario y endocarditis; su susceptibilidad a ampicilina supera el 90 %, aunque pueden emerger variantes con bombas de eflujo activas.13
Algunos de estas opciones terapéuticas las pondremos a continuación con sus respectivas dosis y presentaciones en Ecuador:
| FÁRMACO | PRESENTACIÓN | DOSIS ADULTO | DOSIS PEDIATRICA |
|---|---|---|---|
| Bencilpenicilina Penicilina G | S.P 1-5 millones UI | 6-24 millones UI/día c/4-6 horas | 100 – 400 mil UI/kg/día C/4-6 h |
| Bencilpenicilina Procaínica | S.P 800.000 UI | 1 vial/ 12-24 h | 25-50 mil UI/kg c/12-24 horas |
| Bencilpenicilina Benzatínica | S.P 600mil UI 1200.000 – 2400.000 UI |
2400000 UI/ 4 semanas | 2-6 años: 600 mil UI 7-12 años: 1200.000 UI |
Creado por autores
| FÁRMACO | PRESENTACIÓN | DOSIS ADULTO | DOSIS PEDRIATRICO |
|---|---|---|---|
| Cefalexina | S.O: 500 mg S.O: 250mg/5 ml |
250-500 mg c/6-12 h | 25-100 mg/kg c/6-12h |
| Cefazolina | S.P: 1g | 250-500 mg IV | 25-100 mg/kg c/8-12h |
| Cefadroxilo | P.S: 250-500mg/5ml | 1 g v/12h | 30 mg/kg c/12 h |
| S.O: 500 mg |
Creado por autores
-
¶ Productoras de β-lactamasa.
Las bacterias Gram positivas productoras de β-lactamasa generan enzimas capaces de hidrolizan el anillo β-lactámico característico de penicilinas naturales y aminopenicilinas, lo que resulta en la neutralización de su actividad, este mecanismo es la causa principal de resistencia en hasta el 80% de aislamientos de Staphylococcus aureus en infecciones de piel y tejidos blandos, y puede coexistir con resistencia mediada por modificación de PBPs en enterococos, la presencia de β-lactamasas de espectro extendido (BLEE) en ciertos estafilococos y enterococos aumentan la complejidad del tratamiento lo que frecuentemente obliga a emplear antibióticos de última línea o combinaciones de inhibidor de β-lactamasa más β-lactámico.¹4
Principales Patógenos.
- Staphylococcus aureus productor de penicilinasa: responsable de forúnculos, celulitis y bacteriemias; hasta 70–80 % de cepas hospitalarias producen β lactamasa.13
- Cepas de Enterococcus faecalis con β lactamasa: implicadas en endocarditis y UTIs complicadas; resistencia variable a ampicilina (10–20 %).13
- Staphylococcus epidermidis nosocomial: coloniza dispositivos intravasculares y prótesis; producción de β lactamasa en 50–60 % de aislamientos, con riesgo de infección persistente.13
Pondremos a continuación las presentaciones y posología de algunos de estos medicamentos que encontramos en Ecuador:
Tabla 4:antibióticos contra bacterias productoras B- Lactamasa.
| FÁRMACO | FORMA | DOSIS ADULTO | DOSIS PEDIATRICA |
|---|---|---|---|
| Amoxicilina + acido clavulánico | S.O: 125+31.25 - 250+62.5 - 500+125 mg/5ml S.P: 1g+ 200mg |
500/125 mg c/12h | -3 meses: 30mg/kg/c 12h +3meses: 45mg/kg/c12h |
| Piperacilina + tazobactam | S.P: 4g/500 mg | Infección intraabdominal: 2g/1.5 g c/6h Neumonía nosocomial: 4.5 g C/6h |
-2 meses: no -40kg: 90 mg/kg/ c8h +40kg: 112.5 mg/kg/IV c8horas |
| Ampicilina + sulbactam | S.P: 1g/0.5g | 15g/3g IV o IM c/6h | +1año -40kg: 200 mg/kg/día +1año +40 kg: 1.5g a 3g c12h |
Creado por autores.
¶ ESTAFILOCOCOS.
Los estafilococos son cocos Gram positivos que se agrupan en racimos y colonizan la piel y mucosas humanas, su virulencia depende de toxinas, enzimas invasivas y la capacidad de formar biopelículas en dispositivos médicos, el tratamiento de elección para cepas sensibles incluye flucloxacilina o cefazolina mientras que en infecciones graves se usan vancomicina o daptomicina, estos estafilococos se clasifican en15:
- No productores de B-lactamasa.
- Mars.
- Vars.
-
¶ No productores de B lactamasa.
Estas cepas carecen de enzimas que hidrolizan penicilinas naturales, por lo que son sensibles a antiestafilocócicos como cloxacilina, oxacilina y cefalosporinas de primera generación, al no producir betalactamasa, las penicilinas convencionales son efectivas, ya que inhiben la síntesis de la pared celular bacteriana al no ser destruidas por enzimas bacterianas, lo que lleva a la lisis celular.16
La penicilina es el tratamiento de elección para infecciones leves y moderadas causadas por estas cepas, en infecciones más graves o cuando se sospecha resistencia, se pueden usar cefalosporinas de 1.ª generación como cefazolina u oxacilina, que son también eficaces contra estos patógenos sin betalactamasa. Aunque menos frecuentes, incluyen variantes de Staphylococcus aureus sensible a meticilina (MSSA) y S. epidermidis susceptible, los principales patógenos incluyen:17
- MSSA: responsable de infecciones cutáneas y bacteriemias.
- S. epidermidis sensible: infecciones asociadas a catéteres.
- S. saprophyticus: cistitis en mujeres jóvenes.
Tabla 5:Fármacos utilizados en bacterias no meticilina ni vancomicina resistentes.
| GRUPO | FÁRMACO | FORMA | DOSIS ADULTO | DOSIS PEDIÁTRICO |
|---|---|---|---|---|
| PENICILINA | Dicloxacilina | S.O: 500 mg L.O: 125- 250 mg/5 ml |
125-500 mg VO cada 6 h (Tomar en ayunas) | < 40 kg: 12.5–25 mg/kg/día VO c/6h Inf. grave: 50–100 mg/kg/día VO c/6h > 40 kg: 125–500 mg VO c/6h |
| CEFALOSPORINA 1ERA GENERACION | Cefazolina | S.P: 1g | 250–500 mg IV c/8h | Bebés y niños: 25–100 mg/kg IV/IM c/8–12h Recién nacidos: 40–60 mg/kg c/8–12h (máx. 1 g) |
| Cefalexina | V.O: 1000 – 750 - 500 mg Suspensión O: 250mg/ml |
Faringitis estreptocócica: 250mg V.O/ 6 horas Celulitis y mastitis: 500 mg V.O/ 6 horas |
<15años: 250mg VO/6horas. >15años: 250mg VO/6horas. |
|
| Cefadroxilo | S.O: 1000-500 Mg Suspensión O: 250-500-125 mg/5ml |
Amigdalitis: 1g V.O/ día. Infecciones del tracto urinario y endocarditis: 2g V.O / dia |
Infecciones susceptibles/Faringitis estreptocócica: 30 mg/kg VO cada día durante10días. | |
| TETRACICLINA DE 2DA GENERACION | Doxiciclina | S.O: 100 mg | 100–200 mg VO/IV día o dividido q12h | ≤ 8 años: No se recomienda > 8 años, < 45 kg: 2.2–4.4 mg/kg/día IV/VO al día |
Creado por autores
-
¶ Estafilococos meticillin resistentes(Mars).
Las MRSA portan el gen mecA que altera PBP2a, reduciendo la afinidad por β lactámicos y ocasionando resistencia a meticilina y otras penicilinas isoxazólicas, el tratamiento de elección son los glicopéptidos (vancomicina) ya que actúa de manera diferente a los betalactámicos, uniéndose a los precursores de la pared celular, si hay resistencia a vancomicina, se pueden usar lipopéptidos (daptomicina) o linezolid en alternativas orales que son opciones eficientes frente a resistencia antimicrobiana, en infecciones comunitarias leves, también se pueden usar TMP-SMX o clindamicina. 18
Tabla 6: Fármacos útiles en bacterias meticillin resistentes (MARS).
| FÁRMACO | PRESENTACIÓN | DOSIS ADULTO | DOSIS PEDIÁTRICO |
|---|---|---|---|
| VANCOMICINA | S.P: 1000 – 500 mg | Enterocolitis estafilocócica: 0.5–2 g/día VO en 6–8 h × 7–10 días Diarrea por C. difficile: 125 mg VO cada 6 h × 10 días Endocarditis infecciosa, septicemia, infecciones de piel, huesos y respiratorias: 500 mg c/6 h o 1 g c/12 h |
Endocarditis infecciosa, septicemia, infecciones de piel, óseas y respiratorias: ≥ 1 mes: 10 mg/kg c/6 h Meningitis bacteriana: 15–20 mg/kg IV c/6 h Otras infecciones: 40 mg/kg/día IV c/6 h |
| TIGECICLINA | Vial: 50 mg IV | Infecciones intraabdominales complicadas, Neumonía adquirida en la comunidad e infecciones complicadas de la piel Inicial: 100 mg de infusión intravenosa, ENTONCES 50 mg de infusión intravenosa cada 12 horas durante 5-14 días |
<18 años: Seguridad y eficacia no establecidas. |
Creado por autores
-
¶ Estafilococos vancomicina resistentes (Vars).
Se trata de una variante de S. aureus que ha adquirido genes de resistencia, en particular el gen** vanA, el cual le permite la capacidad de evadir la acción de la vancomicina, antibiótico que históricamente se usa contra cepas resistentes a meticilina (MRSA).19
Los casos de VRSA son poco frecuentes a nivel mundial, pero representan una gran amenaza porque limitan aún más las opciones terapéuticas, frente a estas cepas, el tratamiento puede incluir antibióticos como linezolid, que inhibe la síntesis proteica sin depender de la pared celular, o daptomicina, que destruye la membrana celular de la bacteria**,** según el perfil de sensibilidad determinado en el antibiograma. 20
Los principales patógenos encontrados son:
- VRSA USA600: aislado clínico reportado en NC, EE. UU. (2021).
- Cepas VISA/hVISA: resistencia intermedia, frecuentes en infecciones persistentes.
- Enterococos portadores de vanA: fuente de genes de resistencia para S. aureus.
Tabla 7: Fármacos útiles ante bacterias vancomicina resistentes(Vars).
| FÁRMACO | PRESENTACIÓN | DOSIS ADULTO | DOSIS PEDIÁTRICO |
|---|---|---|---|
| LINCOMICINA | L.P: 600 mg/2ml | IM: 600 mg c/12–24 h IV: 600–1000 mg c/8–12 h (máx. 8 g/día) |
< 1 mes: Seguridad y eficacia no establecidas > 1 mes de edad: IV: 10–20 mg/kg/día divididos c/8–12 h IM: 10 mg/kg c/12–24 h |
| S.O: 500 mg | |||
| LINEZOLIDA | S.O: 600 mg | Infecciones por enterococos resistentes a la vancomicina e infecciones complicadas de la piel: 600 mg VO/IV c/12 h durante 14–28 días | Infecciones complicadas de la piel y estructuras cutáneas: < 12 años: 10 mg/kg VO/IV c/8 h × 10–14 días ≥ 12 años: 600 mg VO/IV c/12 h × 10–14 días |
| L.P: 2mg/ml |
Creado por autores.
¶ GRAM NEGATIVAS
Las bacterias gramnegativas poseen una estructura más compleja que incluye una membrana externa que funciona como barrera protectora contra múltiples antibióticos esta membrana contiene lipopolisacáridos y se combina con una capa delgada de peptidoglicano lo que les otorga resistencia intrínseca a diversos fármacos y la capacidad de generar endotoxinas además muchas de estas bacterias producen betalactamasas que son enzimas capaces de inactivar antibióticos betalactámicos complicando significativamente el tratamiento las cepas Gram negativas resistentes a antibióticos de amplio espectro causan infecciones graves y de manejo clínico complejo entre los patógenos más relevantes se encuentran Escherichia coli, Klebsiella pneumoniae y Pseudomonas aeruginosa.21
-
¶ No productoras de B lactamasa.
Estas cepas carecen de la capacidad de sintetizar enzimas β lactamasas, lo que lo hace susceptibles a penicilinas y cefalosporinas de amplio espectro, la ausencia de este mecanismo de resistencia permite que dichos antibióticos actúen eficientemente interfiriendo en la síntesis de la pared celular de la bacteria, en estos casos, las opciones terapéuticas puede incluir penicilinas semisintéticas como amoxicilina o ampicilina, o cefalosporinas de primera a tercera generación ( aunque las de primera generación solo son útiles en casos de escherichiacoli, klebsiella pneumoniae y proteus mirabilis), como cefalexina, cefuroxima o ceftriaxona, también se pueden emplear fluoroquinolonas como ciprofloxacina o levofloxacina.22
Tabla 8: Gram negativas no productoras de B-lactamasa.
| GRUPO | FÁRMACO | PRESENTACIÓN | D. ADULTO | D. PEDIÁTRICO |
|---|---|---|---|---|
| CEFALOSPORINAS | Ceftriaxona | S.P: 1000 mg – 500 mg | 1–2 g/día o c/12 h IV | 50–100 mg/kg IM en dosis única |
| Cefotaxima | S.P: 1 g | Sin complicaciones: 1 g IV c/12 h Moderado a severo: 1–2 g IV c/8 h Más graves: 2 g IV cada 6–8 h |
<12 años o <50 kg: 50–200 mg/kg/día IV/IM dividido cada 6–8 h >12 años o >50 kg: 1–2 g IV/IM cada 8 h |
|
| AMINOGLUCOSIDO | Gentamicina | L.P: 10-20-40-40-140 mg/ml | 3–5 mg/kg/día IV/IM dividido c/8 h | Lactantes: 2,5 mg/kg/dosis IV/IM c/8 h Niños y adolescentes: 2–2,5 mg/kg/dosis IV/IM c/8 h |
| AMINOGLUCOSIDO | Amikacina | L.P: 50-250 mg/ml 250-500 mg 1-1.25 g |
15 mg/kg/día dividido IV/IM cada 8–12 h | 15–22,5 mg/kg/día IV/IM dividido c/8 h |
| UREIDOPENICILINAS | Piperacilina + tazobactam | S.P: 4000 + 500 mg | 2-24 g IV | <2 meses: Seguridad y eficacia no establecidas Meses: ≤40 kg: 90 mg/kg >9 meses: >40 kg: 3,375 g IV cada 6 horas |
| AMINOPENICILINAS | Amoxicilina | S.O: 500 – 1000 mg Suspensión O: 125 – 250/5ml |
250-500mg c/8-12h |
>3 meses y <40 kg: 25 mg/kg/día VO dividido cada 12 horas >40 kg: 500 mg VO cada 12 horas o 250 mg VO cada 8 horas |
| Ampicilina | S.O: 250 – 500 - 1000mg Suspensión O: 125-250mg/5ml S.P: 1g |
250-500mg c/6h | 3-6,25mg/kg/c/6h | |
| CARBOXIPENICILINAS | Carbepenicilina | No se encuentra en Ecuador | 250-500 mg c/6h | 50 a 100 mg/kg c/6h |
Creado por autores
-
¶ Productoras de β-Lactamasa.
Los microorganismos resistentes a antibióticos β-lactámicos se clasifican según el tipo de enzima β-lactamasa que producen: BLEE y no BLEE.23
Bacterias Productoras de β-Lactamasas (no BLEE).
Las bacterias productoras de β-lactamasas clásicas, como TEM-1 o SHV-1, constituyen un mecanismo de resistencia común. Estas enzimas poseen la capacidad de inactivar eficazmente las penicilinas naturales y antiestafilocócicas. Sin embargo, una estrategia terapéutica fundamental para vencer esta resistencia es el uso de combinaciones de un antibiótico β-lactámico con un inhibidor de β-lactamasa, como el ácido clavulánico o el tazobactam. Estos inhibidores bloquean la acción enzimática, permitiendo que el antibiótico recupere su efectividad. Combinaciones como amoxicilina + ácido clavulánico o piperacilina + tazobactam son pilares del tratamiento. Además, las cefalosporinas de segunda o tercera generación suelen mantener su actividad frente a estas enzimas.23
Dentro de este grupo las bacterias principales encontramos:
- Escherichia coli: Infecciones urinarias, intestinales y sepsis.
- Klebsiella pneumoniae: Neumonías, otitis y exacerbaciones de bronquitis.
- Proteus mirabilis: Infecciones urinarias y de heridas.
- Moraxella catarrhalis: Exacerbaciones de bronquitis y otitis media.24
Tabla 9: Bacterias No Blee (betalactamasas de espectro extendido).
Creado por autores
-
¶ Bacterias productoras de β-Lactamasa de espectro extendido (Blee).
Las betalactamasas de espectro extendido (BLEE) representan un desafío clínico significativamente mayor. Estas enzimas, que suelen ser derivadas mutantes de las clásicas, tienen la capacidad ampliada de degradar no solo las penicilinas, sino también las cefalosporinas de amplio espectro y el monobactam aztreonam. 25
Según la clasificación funcional de Bush-Jacoby-Medeiros, la mayoría de las BLEE se engloban en el Grupo 2be (Clase A), caracterizado por su espectro extendido y por ser inhibidas por el ácido clavulánico. Esta capacidad de hidrolizar los antibióticos β-lactámicos más potentes deja muy pocas opciones terapéuticas. Por ello, el tratamiento de elección para las infecciones graves causadas por estos microorganismos son los carbapenémicos, debido a su alta estabilidad frente a la hidrólisis por BLEE. Para casos de resistencia a carbapenémicos o en infecciones leves, se pueden emplear alternativas como la fosfomicina o la tigeciclina. 26
Tabla 10: Bacterias β-Lactamasa de espectro extendido (Blee).
| GRUPO | FÁRMACO | PRESENTACIÓN | DOSIS |
|---|---|---|---|
| CARBAPENIMICOS | Imipenem + cilastatina | S.P: 500mg + 500 mg | 500 mg IV cada 6 horas |
| Ertapenem | S.P: 1g | 1 g/día IV/IM hasta 14 días | |
| Meropenem | S.P: 1g – 500 mg | 1 g IV c/8h | |
| FLUOROQUINOLONAS | Moxifloxacino | S.O: 400 mg | 400 mg IV c/24h |
| Ciprofloxacino | S.O: 500 mg L.P: 2 mg/ml |
400 mg IV c/12h |
Creado por autores
¶ BACTERIAS ANAEROBIAS.
Las infecciones por bacterias anaerobias, tanto Gram positivas como Gram negativas, representan una parte significativa de las enfermedades infecciosas en la práctica clínica, especialmente en contextos quirúrgicos, infecciones intraabdominales, ginecológicas, del tracto respiratorio inferior y en abscesos profundos, el tratamiento empírico debe considerar la flora polimicrobiana característica de estas infecciones, así como la localización anatómica y la posibilidad de resistencia antimicrobiana.27
El metronidazol se posisiona como un agentes antimicrobianos de primera línea para el tratamiento de infecciones por causadas por anaerobios, tanto Gram negativos como Gram positivos, este fármaco demuestra una excelente actividad excepcional contra anaerobios Gram negativos obligados, como Bacteroides fragilis, Fusobacterium spp., y también frente a grampositivos como Clostridium spp., incluyendo C. difficile, sin embargo, su espectro es limitado frente a anaerobios grampositivos no formadores de esporas como Peptostreptococcus spp., por lo que su uso debe acompañarse de otros antibióticos en infecciones mixtas.28
De manera complementaria, la clindamicina es un antibiótico lincosamídico que actúa inhibiendo la síntesis proteica al unirse a la subunidad ribosomal 50S, tiene una cobertura eficaz contra bacterias anaerobias Gran positivas, incluyendo Clostridium perfringens, diversas especies de Peptostreptococcus spp., aso como otros cocos Gram positivos de carácter anaerobios, además demuestran actividad a algunas cepas de Propionibacterium acnes.29
Tabla 11:Fármacos útiles ante bacterias anaerobias.
| GRUPO | FÁRMACO | PRESENTACIÓN | D. ADULTO | D. PEDIÁTRICO |
|---|---|---|---|---|
| LINCOSAMIDAS | Clindamicina | L.P: 600mg/4ml S.O: 300 mg Óvulos: 100 mg |
Infecciones: IV o IM 600 – 1200 mg/día | Infecciones orofaríngeas: 10 – 20 mg/kg/día Infecciones: <1 mes: 15-20 mg/kg/día 1 mes-16 años: 20-40 mg/kg/día |
| NITROIMIDAZOLES | Metronidazol | S.O: 250-500 mg L.O: 125-250 mg/5ml L.P: 500 mg |
Infecciones bacterianas: De carga: 15 mg/kg De mantenimiento: 7.5 mg/kg/cd 6h |
Infecciones bacterianas: 30mg/kg/día |
| Tinidazol | S.O: 1g S. vaginal: 150 mg |
2 g/día VO durante 3 días | ¶ < 3 años: Seguridad y eficacia no establecidas¶ >3 años: 50 mg/kg/día VO |
|
| PENICILINA | Penicilina G 8 no bacteriodes fgragilis) | S.P: 2400000 - 1200000 – 600000 UI | 1.2 - 2.4 mill cada 28 días | 2-6 años:600 mil 7-12 años: 1.2 mill >12 años: 2.4 mill |
| Amoxicilina + ácido clavulánico ( no bacteroides fragilis). | S.O: 125+31.25 - 250+62.5 - 500+125 mg/5ml S.P: 1g+ 200mg |
500/125 mg c/12h | -3 meses: 30mg/kg/c 12h +3meses: 45mg/kg/c12h |
|
| Piperacilina/tazobactam | Viales: Piperacilina 4g + tazobactam 0,5 g | Rango de dosis habitual IV: 3-4 g/dosis cada 4-6 h; no exceder los 24 g/24 horas IM: 2-3 g/dosis cada 6-12h; no exceder los 24 g/24 horas Vías Urinarias, Sin complicaciones 6-8 g/día IV/IM (100 a 125 mg/kg/día) dividido cada 6-12 h Neumonía adquirida en la comunidad 6-8 g/día IV/IM (100 a 125 mg/kg/día) dividido cada 6-12 h Colangitis aguda 4 g IV cada 6 horas Infecciones moderadas 2-3 g/dosis IV/IM cada 6-12 h; no exceder de 2 g IM/sitio |
Rango de dosis habitual Neonatos: 100 mg/kg IV/IM cada 12 horas Bebés y niños: 200-300 mg/kg/día IV/IM divididos cada 4-6 horas Fibrosis quística 350-500 mg/kg/día IV/IM dividido cada 4-6 horas |
|
| CARBAPENÉMICOS | Imipenem + cilastarina | S.P: 500 + 500 mg | 500 – 750 mg cada 12 h | <1 semana, >1,5 kg: 25 mg/kg IV cada 12 horas 1-4 semanas, >1,5 kg: 25 mg/kg IV cada 8 horas 4 semanas-3 meses, >1,5 kg: 25 mg/kg IV cada 6 horas >3 meses: 15-25 mg/kg IV cada 6 >12 años: 10-15 mg/kg IV cada 6 horas |
| Meropenem | S.P: 1000 – 500 mg | 500mg -1g cada 8h | Meningitis bacteriana: ≥3 meses: 40 mg/kg IV cada 8 horas Infecciones intraabdominales complicadas: ≥3 meses: 20 mg/kg IV cada 8 horas |
|
| Ertapenem (actualmente no aprobado por la FDA) | S.P: 1g | 1 g c/24h |
3 meses - 12 años: 15 mg/kg IV/IM cada 12 horas |
|
| TETRACICLINAS | Doxiciclina | S.O: 100 mg | 100 mg/día | >8 años, <45 kg: 4,4 mg/kg/día VO/IV dividido cada 12 horas >8 años, ≥45 kg: 100 mg VO cada 12 horas o 50 mg VO cada 6 horas el día |
¶ PSEUDOMONAS.
El tratamiento empírico de infecciones por Pseudomonas aeruginosa representa un desafío clínico debido a su alta resistencia intrínseca y adquirida frente a múltiples clases de antimicrobianos, este bacilo Gram negativo no fermentador es un patógeno oportunista prevalente en entornos hospitalarios, especialmente en pacientes inmunocomprometidos, con dispositivos invasivos o bajo tratamientos antibióticos prolongados.30
En pacientes neutropénicos con fiebre persistente, el manejo empírico se inicia con monoterapia utilizando ceftazidima o un carbapenémico como imipenem o meropenem, pero en contextos de alto riesgo de resistencia como sepsis grave, bacteriemia asociada a dispositivos o neutropenia hospitalaria, se recomienda terapia combinada con dos agentes activos contra Pseudomonas aeruginosa de clases diferentes, como la combinación de un betalactámico antipseudomónico (piperacilina-tazobactam, cefepima o ceftazidima) con un aminoglucósido (amikacina o tobramicina) o una fluoroquinolona (ciprofloxacino), estrategia que proporciona sinergia bactericida y reduce la probabilidad de selección de cepas resistentes durante el tratamiento.30
Tabla 12: Fármacos útiles en el tratamiento de infecciones por Pseudomonas.
| FÁRMACO | PRESENTACIÓN | D. ADULTO | D. PEDIÁTRICO |
|---|---|---|---|
| AMIKACINA | L.P: 250 mg – 500 mg – 1 g – 1.25 g |
15 mg/kg/día dividido cada 8 horas | <1 días: 18 mg/kg/cada 48 h Mayor a 7 días: 15 mg/kg/día |
| MEROPENEM | S.P: 500 mg – 1 g | 500 – 1 g cada 8 horas |
+3 meses: 10 mg/kg/ cd 8 horas |
| TOBRAMICINA | S.O: 28 mg L.I: 300 mg/ 5 ml |
3-6 mg/kg/día | <5años: 2.5 mg/kg/ cd 8 horas +5 años: 2-2.5 mg/kg/cd 8 horas |
| PIPERACILINA + TAZOBACTAM | L.P: 4000 mg/500mg | 4.5 g cada 8 horas | - 9 meses: 80mg + 10 mg cada 6 horas +9 meses: 100 mg + 12.5 mg cada 6 horas |
| CEFTAZIDIMA + AVIBACTAM | S.P: 2 g + 0.5 g | 2.5 g cada 8 horas infundido por 2 horas | <28 días a De 3 a <6 meses: ceftazidima 40 mg/kg y avibactam 10 mg/kg IV cada 8 horas De 6 meses a <2 años: ceftazidima 50 mg/kg y avibactam 12,5 mg/kg IV cada 8 horas |
| CIPROFLOXACINO | S.O: 500 mg L.P: 20mg/2 ml – 10mg/ml |
400 mg cada 8 horas | <1 año: Seguridad y eficacia no establecidas ≥1 año: 6-10 mg/kg cada 8 horas; durante 10-21 días ≥1 año: 10-20 mg/kg cada 12 horas cada 12 horas durante 10-21 días |
Elaborado por autores.
Finalmente, es relevante destacar que fármacos como la clindamicina y el metronidazol, aunque útiles en infecciones mixtas o anaeróbicas, no poseen actividad contra Pseudomonas aeruginosa, y su uso en este contexto debe ser evaluado cuidadosamente para evitar fallas terapéuticas.31
¶ ACINETOBACTER.
El género Acinetobacter, en particular Acinetobacter baumannii, representa un desafío terapéutico creciente dentro del ámbito hospitalario, debido a su capacidad para desarrollar y adquirir múltiples mecanismos de resistencia, este microorganismo Gram negativo no fermentador ha sido implicado en infecciones nosocomiales graves, como neumonía asociada a ventilador, bacteriemias, infecciones de heridas quirúrgicas y del tracto urinario, con alta prevalencia en unidades de cuidados intensivos.32
El tratamiento empírico contra Acinetobacter spp. debe iniciarse precozmente ante la sospecha clínica fundada, especialmente en pacientes críticos, con antecedentes de estancia hospitalaria prolongada o uso reciente de antibióticos de amplio espectro,en estos casos, se recomienda una terapia combinada inicial, ajustada posteriormente según el resultado del cultivo y antibiograma.33
Entre los antibióticos efectivos contra A. baumannii, los carbapenémicos han representado históricamente la primera línea de tratamiento, sin embargo, la emergencia global de cepas resistentes a carbapenémicos ha impulsado el uso de alternativas menos convencionales.34
En contextos donde la resistencia a carbapenémicos es elevada, se han empleado antibióticos como colistina, tigeciclina, sulbactam y combinaciones de estos agentes, la colistina, a pesar de su nefrotoxicidad, ha sido rescatada como una opción terapéutica en infecciones por Acinetobacter multirresistente.35
| FÁRMACO | PRESENTACIÓN | D. ADULTO | D. PEDIÁTRICO |
|---|---|---|---|
| AMIKACINA | L.P: 250 mg – 500 mg – 1 g – 1.25 g |
15 mg/kg/día dividido cada 8 horas | <1 días: 18 mg/kg/cada 48 h Mayor a 7 días: 15 mg/kg/día |
| MEROPENEM | S.P: 500 mg – 1 g | 500 – 1 g cada 8 horas |
+3 meses: 10 mg/kg/ cd 8 horas |
| SULBACTAN + DURLOBACTAM | No disponible en Ecuador | 2 g IV cada 6 horas infundidos durante 3 horas | Seguridad y eficacia no establecida |
| COLISTINA | S.O: 100 mg | 2.5 – 5 mg/kg/ día divido cada 6 -12 horas | Seguridad y eficacia no establecida |
| TIGECICLINA | S.P: 50 ml | I.V 50 mg cada 12 horas | Seguridad y eficacia no establecida |
Creado por autores.
El enfoque terapéutico debe ser individualizado, evaluando factores como el estado inmunológico del paciente, el sitio de la infección, las condiciones locales de resistencia y la disponibilidad de antibióticos, el tratamiento empírico debe transformarse en dirigido tan pronto como se obtengan los resultados microbiológicos, evitando el uso prolongado de antimicrobianos de amplio espectro y previniendo la toxicidad asociada, especialmente en el caso de colistina y aminoglucósidos.36
¶ BACTERIAS INTRACELULARES.
Las bacterias intracelulares son microorganismos que requieren de células huésped para replicarse y sobrevivir, esta característica le proporciona una ventaja frente al sistema inmune y a algunos antibióticos, entre las bacterias intracelulares más relevantes desde el punto de vista clínico se encuentran Legionella pneumophila, Chlamydia trachomatis, Chlamydia pneumoniae y Mycoplasma pneumoniae, las cuales son responsables de infecciones respiratorias, urogenitales y sistémicas37.
Legionella pneumophila es una bacteria gramnegativa de carácter facultativo, cuya principal via de transmisión es la inhalación procedente de agua contaminada, dado su carácter intracelular obligado, el tratamiento debe priorizar que el antibiótico penetre adecuadamente dentro de los macrófagos, donde se incluyen macrólidos (azitromicina y claritromicina), fluoroquinolonas (levofloxacina y moxifloxacina), y doxiciclina, que ha mostrado eficacia en casos moderados 38 .
Por otro lado, Chlamydia trachomatis, una bacteria gramnegativa e intracelular obligada, es responsable de infecciones de transmisión sexual como uretritis, cervicitis y enfermedad pélvica inflamatoria, así como de conjuntivitis neonatal, el tratamiento de elección incluye antibióticos que actúan dentro de las células, siendo la azitromicina y la doxiciclina los más utilizados 39.
Chlamydia pneumoniae, también intracelular obligada, causa infecciones respiratorias atípicas, tales como faringitis, bronquitis y neumonía leve y el tratamiento sigue siendo similar al de otras clamidias, utilizando antibióticos como azitromicina, claritromicina, doxiciclina y levofloxacina, dependiendo de la severidad de la infección y las características del paciente 40.
Mycoplasma pneumoniae, una bacteria sin pared celular, también es responsable de neumonías atípicas, faringitis y bronquitis, especialmente en adolescentes y adultos jóvenes, en su tratamiento, se utilizan macrólidos como azitromicina, claritromicina y eritromicina, así como tetraciclinas como doxiciclina y fluoroquinolonas respiratorias como levofloxacina 41.
Tabla 14:Fármacos a utilizar ante bacterias intracelulares.
| FAMILIA | FÁRMACO | PRESENTACIÓN | DOSIS ADULTO | DOSIS PEDIÁTRICO |
|---|---|---|---|---|
| MACRÓLIDOS | Azitromicina | S.O: 500 mg L.O: 200 mg/ 5ml |
NAC, Faringitis y Amigdalitis, Infecciones no complicadas de la piel: 500 mg VO x 1 dosis el día 1, seguido de 250 mg VO qDay los días 2-5 EPOC y Sinusitis bacteriana aguda 500 mg VO una vez al día durante 3 días Uretritis y cervicitis no gonocócicas 1 gramo por VO x 1 dosis |
NAC <6 meses: Seguridad y eficacia no establecidas ≥6 meses: 10 mg/kg VO x 1 dosis el día 1, seguido de 5 mg/kg VO los días 2 a 5 Faringitis/Amigdalitis <2 años: Seguridad y eficacia no establecidas ≥2 años: 12 mg/kg VO una vez al día durante 5 días; sin exceder los 500 mg/día |
| Claritromicina | L.P: 500 mg/5ml S.O: 125-250-500 mg |
NAC y faringitis o amigdalitis: 250 mg V.O cada 12 horas Sinusitis maxilar: 500 mg V.O cada 12 horas |
NAC
≥3 meses: 15 mg/kg/día VO dividido cada 12 horas durante 10 días; |
|
| Eritromicina | S.O: 200-250-400 mg/5ml 500 mg |
250-500 mg c/6-12h max: 4gr | Seguridad y eficacia no establecida | |
| TETRACICLINAS | Doxiciclina | S.O: 100 mg | 100–200 mg VO/IV día o dividido q12h | ≤ 8 años: No se recomienda > 8 años, < 45 kg: 2.2–4.4 mg/kg/día IV/VO al día |
| Tetraciclina | S.O: 250 – 500 mg | 500 mg cada 12 h | ≤8 años: No recomendado >8 años: 25-50 mg/kg/día VO dividido cada 6 horas |
|
| FLUOROQUINOLONAS | Levofloxacina | S.O: 500 mg L.P: 5mg/ml |
NAC y sinusitis bacteriana aguda, infecciones de la piel: 500 mg VO/IV 1 vez al día ITU: 250 mg VO/IV 1 vez al día Infecciones complicadas del tracto urinario/pielonefritis: 250 mg VO/IV 1 vez al día o 750 mg VO/IV 1 vez al día |
Seguridad y eficacia no establecida |
| Moxiflozacino | S.O: 400 mg Sol. iny 400mg/100ml 400mg/250ml |
400mg VO/VI c/día | Seguridad y eficacia no establecida | |
| LINCOSAMIDAS | Clindamicina | L.P: 600mg/4ml S.O: 300 mg Óvulos: 100 mg |
Infecciones: IV o IM 600 – 1200 mg/día | Infecciones orofaríngeas: 10 – 20 mg/kg/día Infecciones: <1 mes: 15-20 mg/kg/día 1 mes-16 años: 20-40 mg/kg/día |
| RIFAMICINAS | Rifampicina | S.O: 300 L.O: 100 mg / 5 ml |
600 mg cada 12 horas | ≤1 mes: 10 mg/kg/día VO dividido cada 12 horas >1 mes: 20 mg/kg/día VO dividido cada 12 horas |
Creado por autores.
El tratamiento de las infecciones causadas por bacterias intracelulares se debe iniciar empíricamente, tomando en cuenta el perfil epidemiológico del paciente, los síntomas clínicos y la farmacocinética de los antibióticos, también debemos tener en cuenta que la selección del tratamiento adecuado depende de factores como la edad del paciente, el contexto clínico y las comorbilidades asociadas 41.
¶ CONCLUSIONES.
La administración empírica de antibióticos representa una intervención terapéutica fundamental y de primera línea en el manejo de infecciones bacterianas graves, ya que un retraso en el tratamiento apropiado se asocia directamente con un incremento en la morbimortalidad, esta revisión demuestra que la elección inicial del régimen antibiótico debe ser un proceso meticuloso y bien fundamentado, integrando la clasificación Gram del presunto patógeno, los patrones epidemiológicos y de resistencia a nivel local, la localización de la infección y las particularidades individuales del paciente.
El examen de las guías clínicas actualizadas de instituciones como la OMS, los CDC y el Ministerio de Salud Pública del Ecuador enfatiza la urgente necesidad de priorizar el uso racional de los antimicrobianos, un enfoque que no solo persigue la eficacia clínica inmediata, sino también preservar la utilidad futura de estos medicamentos mediante la mitigación de la resistencia antimicrobiana, debido al uso indiscriminado de antibióticos de amplio espectro, especialmente aquellos considerados de último recurso como los carbapenémicos y la colistina, acelera la aparición y diseminación de cepas multirresistentes, entre ellas Pseudomonas aeruginosa, Acinetobacter baumannii y Enterobacterias productoras de BLEE y carbapenemasas, lo que nos sitúa al borde de una crisis de salud pública.
En consecuencia, se concluye que la reevaluación sistemática a las 48-72 horas constituye el pilar central para el éxito de la terapia empírica, este desescalamiento guiado por los resultados microbiológicos y la respuesta clínica del paciente resulta la estrategia más efectiva para optimizar el tratamiento, minimizar eventos adversos y reducir la presión selectiva que impulsa la resistencia, la implementación de programas de optimización de antimicrobianos y la adherencia rigurosa a protocolos institucionales basados en evidencia local son acciones indispensables para promover una prescripción prudente y asegurar la sostenibilidad del arsenal antibiótico disponible para las generaciones futuras.
¶ BIBLIOGRAFIA.
- Clinical and Laboratory Standards Institute. Performance standards for antimicrobial susceptibility testing. 31st ed. CLSI supplement M100 [Internet]. 2021 [cited 2025 Sep 21]. Available from: https://clsi.org/standards/products/microbiology/documents/m100/
- Eyler RF, Shvets K. Clinical pharmacology of aminoglycosides. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2024 [cited 2025 Sep 21]. Available from: https://www.ncbi.nlm.nih.gov/books/NBK549905/
- Bush K, Bradford PA. Epidemiology of β-lactamase-producing pathogens. Clin Microbiol Rev [Internet]. 2020 [cited 2025 Sep 21];33(2):e00047-19. Available from: https://journals.asm.org/doi/10.1128/CMR.00047-19
- World Health Organization. Global antimicrobial resistance and use surveillance system (GLASS) report [Internet]. Geneva: WHO; 2021 [cited 2025 Sep 21]. Available from: https://www.who.int/publications/i/item/9789240027336
- Nation RL, et al. Updated guidelines for optimized use of the polymyxins. Lancet Infect Dis [Internet]. 2021 [cited 2025 Sep 21];21(3):e68-e80. Available from: https://www.thelancet.com/journals/laninf/article/PIIS1473-3099(20)30677-0/fulltext
- Silverman JA, et al. Contemporary perspectives on daptomycin resistance in Staphylococcus aureus. Nat Rev Microbiol [Internet]. 2023 [cited 2025 Sep 21];21(4):245-59. Available from: https://www.nature.com/articles/s41579-022-00833-7
- Chambers HF, DeLeo FR. Evolution of MRSA: new challenges in management. N Engl J Med [Internet]. 2022 [cited 2025 Sep 21];387(15):1409-21. Available from: https://www.nejm.org/doi/full/10.1056/NEJMra2204402
- Centers for Disease Control and Prevention. Antimicrobial resistance threat report [Internet]. Atlanta: CDC; 2023 [cited 2025 Sep 21]. Available from: https://www.cdc.gov/drugresistance/biggest-threats.html
- Zahari NI, Engku ARA. A review of the resistance mechanisms for β-lactams among Streptococcus pneumoniae. Microb Drug Resist [Internet]. 2023 [cited 2025 Sep 21];29(2):123-36. Available from: https://www.liebertpub.com/doi/10.1089/mdr.2022.1021
- Chen CJ, Huang YC. New antimicrobials for Gram-positive sustained infections: a comprehensive guide. Antibiotics (Basel) [Internet]. 2022 [cited 2025 Sep 21];11(12):1710. Available from: https://www.mdpi.com/2079-6382/11/12/1710
- Smith TL, et al. An update on treatment options for MRSA-related bloodstream infections. Infect Dis Ther [Internet]. 2022 [cited 2025 Sep 21];11(6):2063-85. Available from: https://link.springer.com/article/10.1007/s40121-022-00706-9
- Wisplinghoff H, et al. Staphylococcus epidermidis: nosocomial pathogenesis. Clin Microbiol Rev [Internet]. 2021 [cited 2025 Sep 21];34(3):e00081-20. Available from: https://journals.asm.org/doi/10.1128/CMR.00081-20
- Lee BJ, et al. Contemporary management of MSSA bacteremia: a systematic review. Clin Infect Dis [Internet]. 2023 [cited 2025 Sep 21];76(5):890-901. Available from: https://academic.oup.com/cid/article/76/5/890/6822000
- Gardete S, Tomasz A. Vancomycin resistance mechanisms in Staphylococcus aureus. Nat Rev Microbiol [Internet]. 2022 [cited 2025 Sep 21];20(5):289-303. Available from: https://www.nature.com/articles/s41579-021-00661-1
- Mansour NA, et al. Efficacy and safety of antibiotics in MRSA infections: a network meta-analysis. Antibiotics (Basel) [Internet]. 2024 [cited 2025 Sep 21];13(12):1197. Available from: https://www.mdpi.com/2079-6382/13/12/1197
- McGuinness WA, et al. Emerging vancomycin resistance mechanisms in Staphylococcus aureus. Lancet Microbe [Internet]. 2023 [cited 2025 Sep 21];4(2):e85-e94. Available from: https://www.thelancet.com/journals/lanmic/article/PIIS2666-5247(22)00323-5/fulltext
- Centers for Disease Control and Prevention. VRSA surveillance and response update. MMWR Morb Mortal Wkly Rep [Internet]. 2024 [cited 2025 Sep 21];73(15):345-50. Available from: https://www.cdc.gov/mmwr/volumes/73/wr/mm7315a1.htm
- Tamma PD, et al. IDSA 2023 guidelines for ESBL-E, CRE, and DTR-P. aeruginosa. Clin Infect Dis [Internet]. 2023 [cited 2025 Sep 21];77(2):187-201. Available from: https://academic.oup.com/cid/article/77/2/187/7145232
- Gutiérrez-Gutiérrez B, et al. Global impact of β-lactam/β-lactamase inhibitor combinations for ESBL infections. Lancet Infect Dis [Internet]. 2022 [cited 2025 Sep 21];22(8):e200-e210. Available from: https://www.thelancet.com/journals/laninf/article/PIIS1473-3099(22)00128-9/fulltext
- Tamma PD, et al. Oral versus intravenous therapy for Gram-negative bacteremia. JAMA [Internet]. 2023 [cited 2025 Sep 21];329(18):1570-80. Available from: https://jamanetwork.com/journals/jama/article-abstract/2804321
- Paterson, D. L., et al. (2023). Management of ceftriaxone-resistant Gram-negative bacteremia in the era of new β-lactams. Clinical Microbiology Reviews [Internet], 36(1), e00098-22. Available from: https://journals.asm.org/doi/10.1128/cmr.00098-22
- Brook I. Anaerobic infections in the 21st century. Clin Microbiol Rev [Internet]. 2022 [cited 2025 Sep 21];35(3):e00079-21. Available from: https://journals.asm.org/doi/10.1128/CMR.00079-21
- Food and Drug Administration (FDA). Drug-resistant infections: current treatment landscape [Internet]. 2023 [cited 2025 Sep 21]. Available from: https://www.fda.gov/drugs/antimicrobial-resistance
- Hirsch EB, Tam VH. Multidrug-resistant Pseudomonas aeruginosa: therapeutic challenges and future directions. Nat Rev Microbiol [Internet]. 2023 [cited 2025 Sep 21];21(8):512-28. Available from: https://www.nature.com/articles/s41579-023-00889-1
- Livermore DM. Contemporary mechanisms of resistance in Pseudomonas aeruginosa. Clin Infect Dis [Internet]. 2023 [cited 2025 Sep 21];76(3):e1022-e1030. Available from: https://academic.oup.com/cid/article/76/3/e1022/6612345
- Peleg AY, et al. Acinetobacter baumannii: current treatment options and vaccine development. Lancet Infect Dis [Internet]. 2022 [cited 2025 Sep 21];22(7):e191-e200. Available from: https://www.thelancet.com/journals/laninf/article/PIIS1473-3099(21)00813-5/fulltext
- Magiorakos AP, et al. Updated international definitions for antimicrobial resistance. Clin Microbiol Infect [Internet]. 2023 [cited 2025 Sep 21];29(1):12-25. Available from: https://www.clinicalmicrobiologyandinfection.com/article/S1198-743X(22)00476-3/fulltext
- Durante-Mangoni E, et al. Management of carbapenem-resistant Acinetobacter baumannii: new therapeutic approaches. Clin Microbiol Rev [Internet]. 2023 [cited 2025 Sep 21];36(2):e00088-22. Available from: https://journals.asm.org/doi/10.1128/cmr.00088-22
- Rodríguez-Hernández MJ, et al. High-dose ampicillin-sulbactam for MDR Acinetobacter: current evidence. J Antimicrob Chemother [Internet]. 2022 [cited 2025 Sep 21];77(8):2025-35. Available from: https://academic.oup.com/jac/article/77/8/2025/6609876
- World Health Organization (WHO). Global priority list of antibiotic-resistant bacteria [Internet]. 2023 [cited 2025 Sep 21]. Available from: https://www.who.int/publications/i/item/9789240041516
- European Medicines Agency (EMA). Guideline on the evaluation of medicinal products indicated for treatment of bacterial infections [Internet]. 2023 [cited 2025 Sep 21]. Available from: https://www.ema.europa.eu/en/documents/scientific-guideline/guideline-evaluation-medicinal-products-indicated-treatment-bacterial-infections-revision-3_en.pdf
- National Institutes of Health (NIH). Antimicrobial resistance research agenda [Internet]. 2023 [cited 2025 Sep 21]. Available from: https://www.niaid.nih.gov/research/antimicrobial-resistance-research-agenda
- Rodríguez-Hernández MJ, Pachón J, Pichardo C, Cuberos L, Ibáñez-Martínez J, Vila J. High-dose ampicillin-sulbactam for MDR Acinetobacter: current evidence. J Antimicrob Chemother [Internet]. 2022 [cited 2025 Sep 21];77(8):2025-35. Available from: https://academic.oup.com/jac/article/77/8/2025/6609876
- Roberts JA, Abdul-Aziz MH, Lipman J, et al. Personalized antibiotic dosing in critically ill patients: current approaches and future directions. Lancet Infect Dis [Internet]. 2023 [cited 2025 Sep 21];23(5):e187-e199. Available from: https://www.thelancet.com/journals/laninf/article/PIIS1473-3099(23)00089-2/fulltext
- Bush K, Bradford PA. Contemporary perspectives on β-lactams and β-lactamase inhibitors. Nat Rev Microbiol [Internet]. 2023 [cited 2025 Sep 21];21(6):385-400. Available from: https://www.nature.com/articles/s41579-023-00874-7
- Zahari NI, Engku ARA. A review of the resistance mechanisms for β-lactams among Streptococcus pneumoniae. Microb Drug Resist [Internet]. 2023 [cited 2025 Sep 21];29(2):123-36. Available from: https://www.liebertpub.com/doi/10.1089/mdr.2022.1021
- Roberts JA, Abdul-Aziz MH, Lipman J, et al. Therapeutic drug monitoring in critical care: optimizing antibiotic therapy. Clin Microbiol Rev [Internet]. 2023 [cited 2025 Sep 21];36(2):e00088-22. Available from: https://journals.asm.org/doi/10.1128/cmr.00088-22
- Chambers HF, DeLeo FR. Evolution of Staphylococcus aureus resistance in the 21st century. N Engl J Med [Internet]. 2023 [cited 2025 Sep 21];388(15):1390-402. Available from: https://www.nejm.org/doi/full/10.1056/NEJMra2204402
- Chopra I, Roberts M. Tetracycline antibiotics: current status and future prospects. Nat Rev Microbiol [Internet]. 2022 [cited 2025 Sep 21];20(8):465-78. Available from: https://www.nature.com/articles/s41579-022-00713-0
- Hooper DC, Jacoby GA. Quinolone resistance: mechanisms and clinical implications. Clin Microbiol Rev [Internet]. 2023 [cited 2025 Sep 21];36(1):e00072-22. Available from: https://journals.asm.org/doi/10.1128/cmr.00072-22
- Mandell GL, Bennett JE, Dolin R. Mandell, Douglas, and Bennett's principles and practice of infectious diseases. 10th ed. Elsevier [Internet]. 2023 [cited 2025 Sep 21]. Available from: https://www.elsevier.com/books/mandell-douglas-and-bennetts-principles-and-practice-of-infectious-diseases/mandell/978-0-443-11273-7
¶ ANEXOS
Ilustración 1 Diana Terapéutica
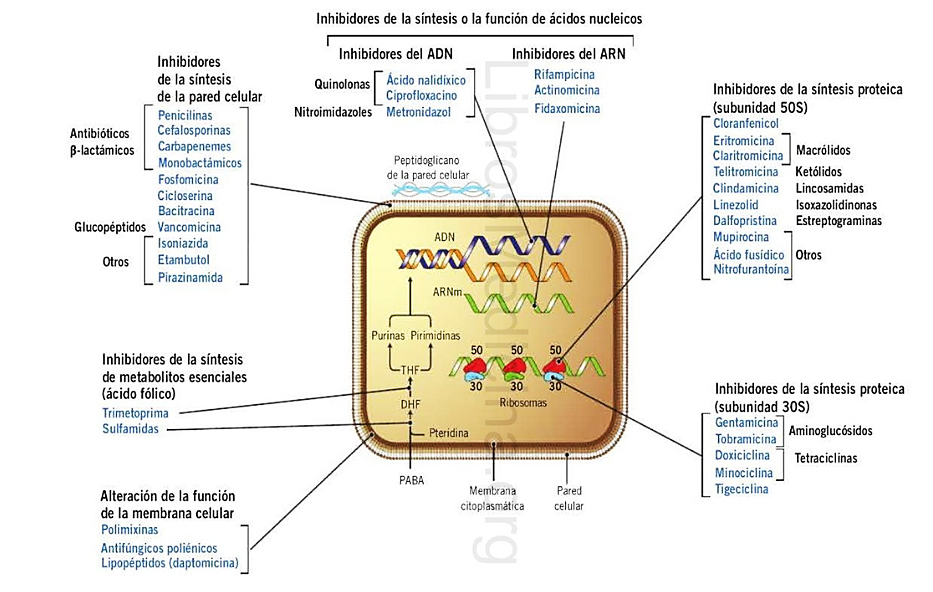
¶ FICHA TÉCNICA
- Créditos: Universidad Técnica de Machala — Facultad de Ciencias Químicas y de la Salud (Carrera de Medicina).
- Asignatura: Terapéutica | Tema: Antimicrobianos en enfermedades bacterianas | Curso: Sexto semestre “B” (Área Clínica).
- Autores: Scarlet N. Balcázar M.; Emily C. Coronado G.; Luis A. Sares M. | Docente: Roberto E. Aguirre Fernández, PhD.
- Machala–El Oro, septiembre de 2025.